某溶液中含有较大量的Cl-、OH-、CO32-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是
①滴加过量Mg(NO3)2;②滴加过量MgCl2;③滴加过量AgNO3溶液;④滴加过量Ba(NO3)2溶液;⑤滴加过量BaCl2溶液;⑥过滤
| A.①⑥④⑥③ | B.②⑥⑤⑥③ |
| C.④⑥①⑥③ | D.⑤⑥②⑥③ |
处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知:CO(g)+ 1/2 O2(g)  CO2(g)∆H=-283.0 kJ/mol
CO2(g)∆H=-283.0 kJ/mol
S(g)+ O2(g) SO2(g)∆H=-296.0 kJ/mol
SO2(g)∆H=-296.0 kJ/mol
下列说法不正确的是:
| A.两个反应均为氧化还原反应 |
| B.CO2与SO2可以用澄清石灰水鉴别 |
| C.CO2分子中各原子最外层均为8电子稳定结构 |
D.相同条件下:2CO(g)+SO2(g)  S(g)+2CO2 (g)∆H=-270kJ/mol S(g)+2CO2 (g)∆H=-270kJ/mol |
锅炉水垢是一种安全隐患,除去水垢中的CaSO4,可先用Na2CO3溶液处理,使之转化为易溶于酸的CaCO3,而后用酸除去。下列说法不正确的是:
| A.CaCO3的溶解度小于CaSO4 |
| B.沉淀转化的实质是沉淀溶解平衡的移动 |
| C.沉淀转化的难易与溶解度差别的大小无关 |
| D.CaSO4到CaCO3的沉淀转化中并存着两个沉淀溶解平衡 |
将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是
| A.与NaOH反应的氯气一定为0.3 mol |
| B.n(Na+):n(Cl-)可能为7:3 |
| C.若反应中转移的电子为n mol,则0.15<n<0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
一定条件下,在体积为VL的密闭容器中,一氧化碳和氢气反应生成甲醇: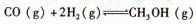
下图表示该反应在不同温度下的反应过程:
关于该反应,下列说法正确的是:()
| A.反应达平衡后,升高温度,平衡常数K增大。 |
| B.反应过程中使用Cu2O/ZnO作催化剂,二者均不参加反应。 |
C.500℃反应达到平衡时,用氢气物质的量浓度减少表示该反应的反应速率是: |
| D.300℃反应达到平衡后,若其他条件不变,将体积缩小到原来的1/2,平衡右移,氢气物质的量浓度增大。 |
某化学兴趣小组对废铁屑做如图所示的处理。相关分析正确的是:
| A.滤液的溶质是Fe(NO3)2 |
| B.该实验中发生的反应都为氧化还原反应 |
| C.沉淀X为Fe(OH)2 |
| D.沉淀X受热分解得到Fe2O3 |