在11Na、12Mg、13Al、14Si、15P、16S、17Cl、18Ar八种元素中,能用 表示核外电子排布的常见阳离子共有
表示核外电子排布的常见阳离子共有
| A.1种 | B.2种 | C.3种 | D.4种 |
下列各对物质中,互为同系物的是
| A.CH4、C2H4 | B.CH4、C2H5OH |
| C.C2H6、C3H8 | D.CH3COOH、C3H6 |
下列化学反应中,能得到单质铝的是
| A.Al2O3与盐酸反应 | B.Al2O3与NaOH反应 |
| C.高温下灼烧Al(OH)3 | D.电解熔融Al2O3 |
下列仪器中, 不能作反应容器的是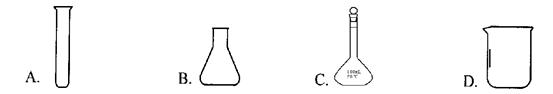
下列关于液氯的说法中,不正确的是
| A.液氯属于混合物 | B.液氯呈黄绿色 |
| C.液氯是一种有色、有味、有毒的液体 | D.液氯能使湿润的红色布条褪色 |
下列电离方程式,不正确的是
| A.KOH==K++OH- | B.CH3COOH==CH3COO- + H+ |
C.NH3·H2O NH4++OH- NH4++OH- |
D.Na2CO3 ="=" 2Na++CO32- |