下列反应既属于化合反应又属于氧化还原反应的是
| A.H2SO4+2NaOH==Na2SO4+2H2O |
B.2NaHCO3 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O |
C.CuO+H2 Cu+H2O Cu+H2O |
D.Cl2 +2Na 2NaCl 2NaCl |
在水溶液中能大量共存的一组离子是
| A.Al3+、Na+、HCO3-、SO42- | B.H+、Fe2+、ClO-、Cl- |
| C.Mg2+、K+、SO42-、NO3- | D.NH4+、Ag+、OH-、Br- |
下列实验现象预测正确的是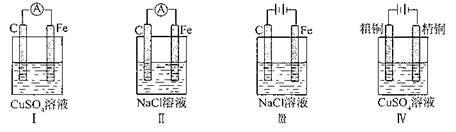
| A.实验I:电流表A指针偏转,碳棒上有红色固体析出 |
| B.实验II:电流表A指针偏转,铁极上有无色气体产生 |
| C.实验III:碳棒上有无色气体产生,铁极上有黄绿色气体产生 |
| D.实验IV:粗铜溶解,精铜上有红色固体析出 |
HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是
| A.0. 1 mol•L-1 HA中c(H+)= c(OH-)+ c(A-) |
| B.0. 1 mol•L-1 HA与 0. 1 mol•L-1NaOH 混合至溶液呈中性:c(Na+)= c(A-) |
| C.0. 1 mol•L-1 NaA 中c(Na+)> c(OH-)>c(A-)> c(H+) |
| D.0. 1 mol•L-1 HA中加入少量NaA固体,HA的电离常数减小 |
短周期元素甲、乙、丙、丁、戊的原子序数依次增大,甲是周期表中原子半径最小的元素,乙形成的气态氢化物的水溶液呈碱性,乙与丁同族,丙、丁、戊同周期,丙单质可制成半导体材料,戊的最高化合价为+7,则
| A.原子半径:乙>丁>丙 |
| B.非金属性:丙>丁>戊 |
| C.甲与戊形成的化合物是共价化合物 |
| D.乙、丙、丁最高价氧化物对应的水化物均是强酸 |
下列离子方程式正确的是
| A.铝溶于NaOH溶液:Al+2OH-=AlO2-+H2↑ |
| B.铜溶于稀硝酸:3Cu+ 8H+ +2NO3-=3Cu2+ +2NO↑ + 4H2O |
| C.碳酸镁中滴加稀盐酸:CO32-+2H+=CO2↑ + H2O |
| D.稀硫酸中滴加氢氧化钡溶液:H++OH-=H2O |