下列除去物质杂质所选试剂或方法不正确的是
| |
物质 |
所含杂质 |
所用试剂 |
方法 |
| A |
O2 |
CO2 |
NaOH溶液 |
洗气 |
| B |
FeSO4 |
CuSO4 |
Fe |
过滤 |
| C |
酒精 |
水 |
CaO |
蒸发 |
| D |
KCl |
K2CO3 |
盐酸溶液 |
蒸发 |
下列化合物在一定的条件下,既能发生消去反应又能发生水解反应的是
| A.①② | B.②③④ | C.①②③④ | D.② |
已知:乙醇可被强氧化剂氧化为乙酸。BrCH2CH=CHCH2Br可经三步反应制取HOOCCHClCH2COOH,发生反应的类型依次是 ()
| A.水解反应、氧化反应、加成反应 | B.加成反应、水解反应、氧化反应 |
| C.水解反应、加成反应、氧化反应 | D.加成反应、氧化反应、水解反应 |
下列物质的核磁共振氢谱图中,有5个吸收峰的是()
A.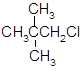 |
B.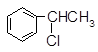 |
C.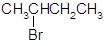 |
D.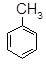 |
要鉴别己烯中是否混有少量甲苯,正确的实验方法是()
| A.先加足量的酸性高锰酸钾溶液,然后再加入溴水 |
| B.先加足量溴水,然后再加入酸性高锰酸钾溶液 |
| C.点燃这种液体,然后再观察火焰的颜色 |
| D.加入浓硫酸与浓硝酸后加热 |
下列有关实验的叙述,正确的是()
| A.用浓氨水洗涤做过银镜反应的试管 |
| B.用分液漏斗分离环己烷和水的混合液体 |
| C.石油分馏时,温度计的水银球插入液面下 |
| D.配制Cu(OH)2悬浊液时,在2mL 10% CuSO4溶液中滴入几滴2%NaOH溶液 |