下列粒子在溶液中能大量共存的是
| A.K+、NO3-、I-、H2SO3 |
| B.Na+、Fe3+、NO3-、CO32- |
| C.Al3+、NO3-、SO32-、OH- |
| D.NH4+、Na+、SO42-、CH3COOH |
下列各组液体混合物,可以用分液漏斗分离的是
| A.乙醇和水 | B.溴乙烷和水 |
| C.溴乙烷和氯仿 | D.苯和溴苯 |
在核磁共振氢谱中出现两组峰,且其面积之比为3∶2的化合物是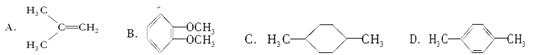
要从乙酸的乙醇溶液中回收乙酸,合理的操作组合是
①蒸馏②过滤③静止分液④加足量钠 ⑤加入足量H2SO4
⑥加入足量NaOH溶液⑦加入乙酸与浓H2SO4混合液后加热 ⑧加入浓溴水
| A.⑦③ | B.⑧⑤② | C.⑥①⑤② | D.⑥①⑤① |
将CH3CHO(易溶于水,沸点为20.8℃的液体)和CH3COOH分离的正确方法是
| A.加热蒸馏 |
| B.加入Na2CO3后,通过萃取的方法分离 |
| C.先加入烧碱溶液之后蒸出乙醛,再加入浓H2SO4,蒸出乙酸 |
| D.和Na反应后进行分离 |
金刚烷的结构如图所示,它可看做是由四个等同的六元环组成的空间构型。请根据中学学过的异构现象判断由氯原子取代金刚烷中的亚甲基(—CH2—)中的氢原子所形成的二氯代物的种类
| A.4种 | B.3种 | C.2种 | D.5种 |