(9分)根据下列氧化还原反应2FeCl3+Cu===2FeCl2+CuCl2设计一个原电池: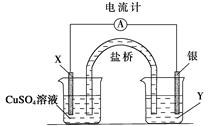
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的________极,发生的电极反应为_________________________;
X电极上发生的电极反应为_________________________;
(3)外电路中的电子是从________电极流向________电极(填具体电极如Ag”)。
如右图所示装置用于测定某碱金属的相对原子质量。仪器本身连同水和干燥管以及其内的无水氯化钙的总质量为480.00 g。现将1.46 g某碱金属单质投入水中,立即用带有干燥管的塞子塞紧瓶口,反应完毕后,测得整套仪器的总质量为481.25 g。该金属元素的相对原子质量是________(结果保留两位小数),若不用干燥管,测得的相对原子质量比实际相对原子质量________(填“偏大”“偏小”或“相等”),理由是________________________________。
25 ℃时,钠的三种化合物的溶解度如下表:
| 化合物 |
NaHCO3 |
Na2CO3 |
NaOH |
| 溶解度/g |
9 |
33 |
110 |
该温度时,用NaOH、水、CaCO3和盐酸为原料制备并从溶液中结晶出33 g纯NaHCO3。
(1)若用水100 g制取时需NaOH多少克?
(2)若用NaOH(s)17.86 g,则需用水_________克。
一定量的液态化合物XY2,在一定量O2中恰好完全反应:XY2(l)+3O2(g)====XO2(g)+2YO2(g),冷却后在标准状况下,测得生成物的体积为672 mL,密度为2.56 g·L-1,则
(1)反应前O2的体积为______________________。
(2)化合物XY2的摩尔质量是_____________________。
(3)在XY2分子中,X、Y两元素质量比为3∶16,则X、Y两元素分别为_____________________和_____________________。(写元素名称)
NH4HCO3与(NH4)2CO3的混合物在受热条件下,均可完全分解生成NH3、CO2、H2O,如果分解产物中NH3、H2O、CO2的物质的量之比为6∶5∶5,那么反应物中NH4HCO3和(NH4)2CO3的物质的量之比为__________。
一包混有杂质的Na2CO3,其中杂质可能是Ba(NO3)2、KCl、NaHCO3中的一种或多种。今取10.6 g样品,溶于水得澄清溶液,另取10.6 g样品,加入足量的盐酸,收集到4.4 g CO2,则杂质是。