如图是广州亚运会开幕式“红棉花开迎宾来”焰火盛宴的一个场景,
请回答下列问题:
(1)焰火利用了部分金属的元素特征的 反应,该反应属于 (填“物理”或“化学”)变化。
(2)现在有一种火焰的引发是当浓H2SO4滴下去跟氯酸钾起作用时,便生成了奇臭的二氧化氯气体,且发现只有氯元素的化合价发生变化。请写出该反应的方程式 。
(3)如图所示的五元环代表A、B、C、D、E五种化合物,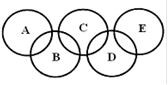
圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素组成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为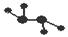 ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
①D的化学式是_________.
②A、B、E中均含有的一种元素名称为______________。
③B的电子式是______________。
④C与纯碱反应的化学方程式为 。
(共20分)
Ⅰ:现有CH4、C2H4、C2H2、C2H6、C3H8五种有机物,回答下列问题:
⑴质量相同时:在相同状况下体积最大的是__ ___,完全燃烧时消耗O2的量最多的是__ _,
⑵同温同压同体积时,五种物质完全燃烧消耗O2的量最多的是__
Ⅱ:有机化学中的反应类型较多,将下列反应归类(填序号)。
①乙苯的制备:
②乙 烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色④乙烯使酸性高锰酸钾溶液褪色
烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色④乙烯使酸性高锰酸钾溶液褪色
⑤由乙烯制聚乙烯⑥甲烷与氯气在光照的条件下反应⑦溴乙烷和氢氧化钠溶液共热
⑧由甲苯制取TNT ⑨往苯酚钠溶液中通入CO2溶液中
(1)其中属于取代反应的是;属于氧化反应的是;
属加成反应的是属于聚合反应的是
(2)写出⑦、⑧、⑨的化学方程式
⑦
⑧
⑨
(1)在下列物质中是同系 物的有;互为同分异构体的有;
物的有;互为同分异构体的有;
互为同素异形体的有;互为同位素的有;属于同一物质的是:
(1)液氯 (2)氯气 (3)白磷 (4)红磷 (5)D (6)T
(3)白磷 (4)红磷 (5)D (6)T
(7) 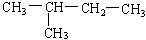 (8)
(8) 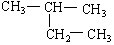
(9)CH2 = CH-CH3(10) 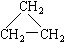 (11)2,2—二甲基丁烷
(11)2,2—二甲基丁烷
(2)、把一端弯成螺旋状的铜丝放在酒精灯火焰加热,看到铜丝表面变_黑,再迅速插入盛乙醇的试管中,看到铜丝 表面 __________;反复多次后,试管中生成有特殊气味的物质,反应的化学方程式为 _____;乙醇所含的官能团的名称______
表面 __________;反复多次后,试管中生成有特殊气味的物质,反应的化学方程式为 _____;乙醇所含的官能团的名称______
在一支试管中放入几小块镁片,把试管放入盛有25℃的饱和石灰水的烧杯中,用胶头滴管滴5ml盐酸于试管中。试回答下列问题:
(提示:Ca(OH)2的溶解度受随温度的升高而降低。)
⑴该试验中观察到的现象是;
⑵产生上述现象的原因是;
(3)写出有关反应的离子方程式;
⑷在上述试验结束后,将试管取出。在烧杯中放入一个小烧杯,小烧杯中放入氢氧化钡晶体和氯化铵晶体的混合物,用玻璃棒搅拌,则观察到的现象是,产生上述现象的原因是。
某温度时,在2L容器中X、Y、Z三种物质的物质的量(n)随着时间(t)变化的曲线如图所示。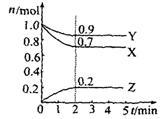
由图中数据分析:
(1)该反应的化学方程式为。
(2)反应开始至2min,用Z表示的平均反应速率为。
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构 造如图所示:A、B两个电极均由多孔的碳块组成。
造如图所示:A、B两个电极均由多孔的碳块组成。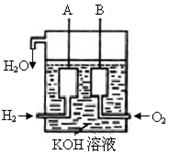
该电池的正极反应式为:;
若该电池工作时增加了1mol H2O,电路中转移电子的物质的量为。
(4)利用反应“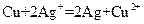 ”设计一个原电池(正极材料用碳棒)。回答下列问题:
”设计一个原电池(正极材料用碳棒)。回答下列问题:
①该电池的负极材料是________,发生________反应(填“氧化”或“还原”),负极的电极反应式为:____________,电解质溶液是________;
②正极上出现的现象是_____________________________;
③若导线上转移电子1  mol,则生成银________g。
mol,则生成银________g。
(14)A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置第周期,第族;
(2)E元素形成的氧化物对应的水化物的化学式为;
(3)元素C、D、E形成的离子半径大小关系是> >
> (用离子符号表示)。
(用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程;
C、D还可形成化合物D2C2,D2C2含有的化学键类型是。
(5)由A、B、C三种元素形成的离子化合物的化学式为;它与强碱溶液 反应的离子方程式是。
反应的离子方程式是。