有一无色溶液,可能含有K+、Al3+、Mg2+、 NH4+、Cl-、SO42-、HCO3—、MnO4—中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量的Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
| A.肯定有Al3+、Mg2+、NH4+、Cl- | B.肯定有Al3+、Mg2+、HCO3— |
| C.肯定有K+、HCO3—、MnO4— | D.肯定有Al3+、Mg2+、SO42- |
下列有机物命名正确的是
| A.2,2,3-三甲基丁烷 | B.2-乙基戊烷 |
| C.2-甲基-1-丁炔 | D.2,2-甲基-1-丁烯 |
常温常压下为无色液体,而且密度大于水的是
①苯 ②硝基苯 ③溴苯 ④四氯化碳⑤溴乙烷⑥乙酸乙酯
| A.①⑥ | B.②③④⑥ | C.②③④⑤ | D.③④⑤⑥ |
pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是 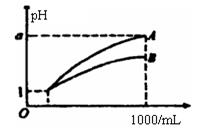
A. A、B两种酸溶液的物质的量浓度一定相等
B. 稀释后,A酸溶液的酸性比B酸溶液的酸性弱
C. 若a=4,则A是强酸,B是弱酸
D. 若1<a<4,则A、B都是弱酸
放热反应CO(g)+H2O(g)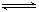 CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。其他条件不变,升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。其他条件不变,升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
| A.若增大CO的浓度,K2和K1都增大 | B.K2>K1 |
| C.c2(CO)=c2(H2O) | D.c1(CO)>c2(CO) |
用物质的量均是0.1 mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),下列对该混合溶液的判断正确的是
| A.c(H+)>c(OH-) |
| B.c(CH3COO-)+c(CH3COOH)=0.1 mol·L-1 |
| C.c(CH3COOH)>c(CH3COO-) |
| D.c(CH3COO-)+c(OH-)=0.1mol·L-1 |