(8分)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式_______ __ ___。
(2)若溶液M由10 mL 2 mol·L-1 NaHA溶液与2 mol·L-1 NaOH溶液等体积混合而得,
则溶液M的pH_ __7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为_ _ __。
(3)若溶液M有下列三种情况:
①0.01 mol·L-1的H2A溶液
②0.01 mol·L-1的NaHA溶液
③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,
则三种情况的溶液中H2A分子浓度最大的为______;pH由大到小的顺序为______。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为________(填“大于、等于、小于”或“均有可能”)。
能源问题日益成为制约经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。

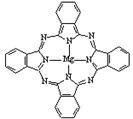
图1图2图3
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的核外电子排布式。
(2)富勒烯衍生物由于具有良好的光电性能。富勒烯(C60)的结构如图1,分子中碳原子轨道的杂化类型为;1 mol C60分子中σ键的数目为。科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图2所示。该化合物中的K原子和C60分子的个数比为。
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、碲化镉及铜铟硒薄膜电池等。
①第一电离能:AsSe(填“>”、“<”或“=”)。
②二氧化硒分子的空间构型为。
(4)金属酞菁配合物可应用于硅太阳能电池中,一种金属镁酞菁配合物的结构如图3,请在图中用箭头表示出配位键的位置。
CuSO4溶液与K2C2O4溶液混合生成一种蓝色钾盐水合物KaCub(C2O4)c·nH2O。通过下述实验确定该晶体的组成。
步骤a:称取0.6720 g样品,放入锥形瓶,加入适量2mol·L-1稀硫酸,微热使样品溶解。再加入30 mL水加热,用0.2000mol·L-1 KMnO4溶液滴定至终点,消耗8.00 mL KMnO4溶液。有关反应:2MnO4-+5C2O42-+16H+=2Mn2++8H2O+10CO2↑
步骤b:接着将溶液充分加热。冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI。用0.2500mol·L-1 Na2S2O3标准溶液滴定至终点,消耗8.00 mL Na2S2O3溶液。滴定时反应为:I2+2S2O32-=2I-+S4O62-
(1)步骤b中生成白色沉淀的离子方程式:。
(2)步骤b中“将溶液充分加热”的目的是。
(3)请完成下列确定样品组成的计算过程。
①计算样品中n (C2O42-)(写出计算过程)
②计算样品中n (Cu2+)(写出计算过程)
③根据原理可求出n (K+),再依据原理求得n (H2O)
④该样品晶体的化学式为
(14分)CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)金刚石和石墨燃烧反应中的能量变化如图所示。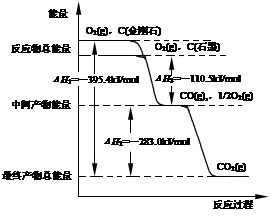
①在通常状况下,金刚石和石墨中,(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为kJ·mol-1。
②石墨与CO2反应生成CO的热化学方程式:。
(2)采用电化学法可将CO2转化为甲烷。试写出以氢氧化钾水溶液作电解质时,该转化的电极反应方程式。
(3)CO2为原料还可合成多种物质。工业上常以CO2(g) 与H2(g)为原料合成乙醇。
①已知:H2O(l)=H2O(g)△H=+44kJ·mol-1
CO(g)+H2O(g) CO2(g)+H2(g)△H=-41.2kJ·mol-1
CO2(g)+H2(g)△H=-41.2kJ·mol-1
2CO(g)+4H2 (g)  CH3CH2OH(g)+H2O(g)△H= -256.1kJ·mol-1。
CH3CH2OH(g)+H2O(g)△H= -256.1kJ·mol-1。
则:2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(l)△H=。
CH3CH2OH(g)+3H2O(l)△H=。
②下图是一种以烟道气为原料合成乙醇的工作原理示意图。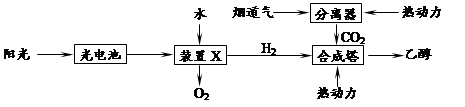
对上述流程的分析,下列说法正确的是。
| A.该流程至少包含4种形式的能量转化 |
| B.装置X中阴极反应为:2H2O-4e-=4H++O2↑ |
| C.合成塔中生成乙醇的反应是化合反应 |
| D.流程设计体现了绿色化学思想 |
③如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。该电池负极的电极反应为。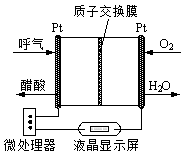
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下: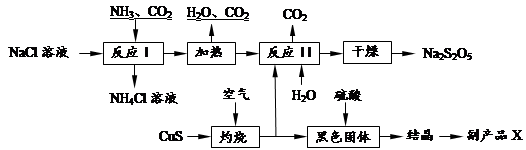
已知:反应Ⅱ包含2NaHSO3 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
(1)实验室制取氨气的化学方程式:。
(2)反应I的化学方程式为:。
(3)“灼烧”时发生反应的化学方程式:。
(4)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:。
(5)副产品X的化学式是。
(6)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为。检验产品中含有碳酸钠杂质所需试剂是(填编号)
①酸性高锰酸钾②品红溶液③澄清石灰水
④饱和碳酸氢钠溶液⑤NaOH⑥稀硫酸
向明矾[KAl(SO4)2·12H2O]溶液中逐滴加入Ba(OH)2溶液至过量。
(1)写出可能发生的有关反应的化学方程式。。
(2)在图中,纵坐标表示生成沉淀的物质的量,横坐标表示加入Ba(OH)2的物质的量。试在图中画出当溶液中明矾为1 mol时,生成的每一种沉淀的物质的量随Ba(OH)2物质的量变化的曲线(在曲线上标明沉淀的化学式)。
(3)向a L物质的量浓度为M mol/L的明矾溶液中滴加物质的量浓度为n mol/L的Ba(OH)2溶液b L,用含a、M、n的表达式表示:
①当b满足________条件时,沉淀的总物质的量为最大值;
②当b满足________条件时,沉淀的质量为最大值。