已知:H2(g)+F2(g)==="2HF(g)" 的能量变化如图所示,下列有关叙述中正确的是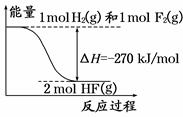
| A.氟化氢气体分解生成氢气和氟气的反应是放热反应 |
| B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ |
| C.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 |
| D.断裂1 mol H—H键和1 mol F—F 键放出的能量大于形成2 mol H—F键放出的能量 |
氮及其化合物的转化具有重要应用。下列说法不正确的是( )
| A. |
实验室探究稀硝酸与铜反应的气态产物:
(稀) |
| B. |
工业制硝酸过程中的物质转化:
|
| C. |
汽车尾气催化转化器中发生的主要反应:
|
| D. |
实验室制备少量
的原理:
|
阅读下列材料,完成下面小题。
氢元素及其化合物在自然界广泛存在且具有重要应用。 、
、 、
、 是氢元素的3种核素,基态
原子
的核外电子排布,使得
既可以形成
又可以形成
,还能形成
等重要化合物;水煤气法、电解水、光催化分解水都能获得
,如水煤气法制氢反应中,
与足量
反应生成
和
吸收
的热量。
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在催化剂作用下与
反应可得到
。我国科学家在氢气的制备和应用等方面都取得了重大成果。
是氢元素的3种核素,基态
原子
的核外电子排布,使得
既可以形成
又可以形成
,还能形成
等重要化合物;水煤气法、电解水、光催化分解水都能获得
,如水煤气法制氢反应中,
与足量
反应生成
和
吸收
的热量。
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在催化剂作用下与
反应可得到
。我国科学家在氢气的制备和应用等方面都取得了重大成果。
(1)下列说法正确的是( )
| A. |
|
| B. |
和 的中心原子轨道杂化类型均为 |
| C. |
分子中的化学键均为极性共价键 |
| D. |
晶体中存在 与 之间的强烈相互作用 |
(2)下列化学反应表示正确的是( )
| A. |
水煤气法制氢: |
| B. |
催化加氢生成
的反应:
|
| C. |
电解水制氢的阳极反应: |
| D. |
与水反应: |
(3)下列物质结构与性质或物质性质与用途具有对应关系的是( )
| A. |
具有还原性,可作为氢氧燃料电池的燃料 |
| B. |
氨极易溶于水,液氨可用作制冷剂 |
| C. |
分子之间形成氢键, 的热稳定性比 的高 |
| D. |
中的 原子与 形成配位键, 具有还原性 |
元素 位于周期表中 族。下列说法正确的是( )
| A. |
原子半径: |
| B. |
第一电离能: |
| C. |
碳单质、晶体硅、 均为共价晶体 |
| D. |
可在周期表中元素 附近寻找新半导体材料 |
实验室制取 的实验原理及装置均正确的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
反应 应用于石油开采。下列说法正确的是( )
| A. |
的电子式为 |
| B. |
中N元素的化合价为 |
| C. |
分子中存在 键 |
| D. |
为非极性分子 |