某一化学兴趣小组的同学在家中进行实验,按照图甲连接好线路,发现灯泡没亮,但是按照图乙接好路线,灯泡亮了。由此得出的以下结论中正确的是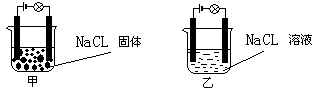
| A.NaCl是非电解质 |
| B.NaCl在水溶液中电离出了可以自由移动的离子 |
| C.NaCl溶液是电解质 |
| D.在NaCl溶液中,水电离出了大量的离子 |
托盘天平两盘内分别放入一个质量相同的烧杯,烧杯里有100 mL 1 mol·L-1H2SO4,天平平衡。向烧杯中加入下列哪些物质经反应后,天平仍保持平衡的是()
| A.各10 g的Mg和Zn |
| B.各1 g的Mg和Zn |
| C.各0.1 mol的Mg和Zn |
| D.6.5 g的Mg,0.1 mol Zn |
将一定质量的锌粉与100 mL 18.5 mol·L-1的浓H2SO4混合,充分反应后锌完全溶解,生成了标准状况下的混合气体33.6 L(设浓H2SO4的还原产物只有SO2,稀硫酸只生成H2),将反应后的溶液稀释成1L时,溶液pH=1,参加反应的锌为 ()
| A.0.9 mol | B.1.2 mol | C.1.5 mol | D.1.8 mol |
两份等体积、等浓度的NaOH溶液,分别与体积相等的MgCl2、AlCl3溶液混合,充分反应后,Mg2+、A3+均恰好形成沉淀,则原MgCl2、AlCl3溶液中Cl-浓度之比为()
| A.1∶1 | B.1∶2 | C.2∶3 | D.3∶2 |
将等物质的量的镁和铝相混合,取四份等质量的该混合物分别加入到足量的下列溶液中,充分反应后,放出氢气最多的是()
| A.3 mol·L-1HCl |
| B.4 mol·L-1HNO3 |
| C.8 mol·L-1NaOH |
| D.18 mol·L-1H2SO4 |
0.1 mol 镁粉分别在足量的O2、CO2、N2中燃烧,生成固体的质量依次为W1、W2、W3,下列关系正确的是()
| A.W2>W1>W3 |
| B.W2=W1>W3 |
| C.W1=W2=W3 |
| D.W3>W2>W1 |