已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1,
Na2O2(s)+CO2(g)===Na2CO3(s)+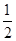 O2(g)ΔH=-226 kJ·mol-1。
O2(g)ΔH=-226 kJ·mol-1。
根据以上热化学方程式判断,下列说法正确的是

| A.CO的燃烧热为283 kJ |
| B.上图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g)ΔH>-452 kJ·mol-1 |
| D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
下列对水体污染物的处理方法中,不正确的是
| A.含H+的废水用中和法处理 | B.含Cu2+、Fe3+的废水用沉淀法处理 |
| C.含有细菌的废水用臭氧杀菌处理 | D.含有重金属离子的废水用明矾处理 |
每年的4月22日为“世界地球日”。某年“世界地球日”的主题是“善待地球”。下列说法中与“世界地球日”的主题无关的是
| A.减少二氧化碳的排放量,以降低温室效应对地球的影响 |
| B.开发利用太阳能、水力发电等无污染能源 |
| C.燃料脱硫以减少酸雨的产生 |
| D.我国政府已向全世界承诺:在全国消灭碘缺乏病 |
下面是小王在医院做的血常规检查报告单的部分内容,小王应该注意补充的微量元素是
| No |
项目 |
结果 |
正常范围参考值 |
单位 |
| 1 |
红细胞计数 |
2.3 |
3.5~5 |
1×1012/L |
| 2 |
血红蛋白 |
75 |
110~150 |
g/L |
| 3 |
血小板计数 |
205.5 |
100~300 |
109/L |
A.锌 B.铁 C.硒 D.碘
下列说法错误的是
A.水华、赤潮、潮汐都是水体富营养化导致的
B.蔬菜、水果类大多为碱性食物,而肉类大多为酸性食物
C.绝大多数食品添加剂在过量使用时对人体是有害的
D.适当多吃鱼类可补充N、C、P、O、H等元素
刚装修好的新房不能立即搬入,因为装修材料中会释放出一些污染物,影响人的身体健康。下面不属于这类污染物的是
| A.二氧化硫 | B.苯 | C.甲苯等 | D.甲醛 |