欲观察环戊烯( )是否能使酸性KMnO4溶液褪色,先将环戊烯溶于适当的溶剂,再慢慢滴入0.005mol·L-1 KMnO4溶液并不断振荡。下列哪一种试剂最适合用来溶解环戊烯做此实验
)是否能使酸性KMnO4溶液褪色,先将环戊烯溶于适当的溶剂,再慢慢滴入0.005mol·L-1 KMnO4溶液并不断振荡。下列哪一种试剂最适合用来溶解环戊烯做此实验
| A.四氯化碳 | B.裂化汽油 | C.甲苯 | D.水 |
工业上常用还原沉淀法处理含铬废水(Cr2 和Cr
和Cr ),其流为:
),其流为:
Cr
 Cr2
Cr2
 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr (黄色)+2H+
(黄色)+2H+ Cr2
Cr2 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)  Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在
下列有关说法中正确的是
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr 浓度增大 浓度增大 |
B.步骤①中当2v(Cr )=v(Cr2 )=v(Cr2 )时,说明反应2Cr )时,说明反应2Cr (黄色)+2H+ (黄色)+2H+ Cr2 Cr2 (橙色)+H2O达到平衡状态 (橙色)+H2O达到平衡状态 |
C.步骤②中,若要还原1 mol Cr2 ,需要12 mol (NH4)2Fe(SO4)2·6H2O ,需要12 mol (NH4)2Fe(SO4)2·6H2O |
| D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽 |
用NA表示,下列说法中正确的有
| A.lmol Na2O2晶体中共含有4NA个离子 |
| B.0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| C.常温常压下16gO2和O3混合气体含有NA个氧原子 |
| D.1mol•L-1的CaCl2溶液中含Cl-的数目为2NA |
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是
| A.KSCN | B.BaCl2 | C.NaOH | D.HCl |
在一密闭容器中有如下反应:L (s) + a G (g)  b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断
b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断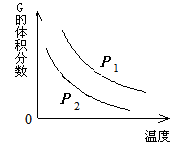
| A.正反应为放热反应 |
| B.化学方程式中的计量数a > b |
| C.G的转化率随温度升高而减小 |
| D.增大压强,容器内气体质量不变 |
设nA为,下列说法正确的是
| A.常温下,28g C2H4含nA个碳碳双键 |
| B.1 mol Cu和足量稀硝酸反应生成nA NO分子 |
| C.常温常压下,22.4L CCl4含有n A个CCl4分子 |
| D.1mol/L NaCl溶液含有n A个Na+ |