在密闭容器中发生下列反应aA(g )cC(g)+d D(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
)cC(g)+d D(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
| A.A的转化率变大 | B.平衡向正反应方向移动 |
| C.a<c+d | D.D的体积分数变大 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.标准状况下,22.4L酒精含有的分子数约为1NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA |
| C.通常状况下,1NA个CO2分子占有的体积为22.4L |
| D.1NA氧原子的质量(以g为单位)在数值上约等于其相对原子质量 |
欲配制100mL1.0mol/LNa2CO3溶液,正确的方法是
| A.将10.6gNa2CO3溶于100mL水中 |
| B.将28.6g Na2CO3·10H2O溶于少量水中,再用水稀释至100mL |
| C.将20mL5.0mol/L Na2CO3溶液用水稀释至100mL |
| D.在20mL5.0mol/L Na2CO3溶液中加入80mL水 |
关于从碘水中分离出碘单质的实验,下列说法正确的是
| A.可以用酒精萃取出碘单质 |
| B.可以用CCl4萃取出碘单质,理由是CCl4密度比水大 |
| C.若用CCl4萃取出碘单质,萃取后下层液体呈紫红色 |
| D.若用CCl4萃取出碘单质,萃取后无色液体层应从分液漏斗的上口倒出 |
下列实验操作中正确的是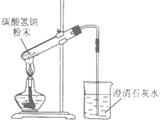
| A.用上图装置加热碳酸氢钠粉末 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.过滤时,若发现滤液浑浊,应更换滤纸,重新过滤 |
| D.制备Fe(OH)3胶体是向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
某合金是由锌铁按照一定比例熔合而成,其中锌的质量分数为72%。某同学取0.1g该合金粉末进行实验,则所取样品所含铁原子数约为
| A.3.01×1020个 | B.6.02×1021个 |
| C.7.74×1020个 | D.6.67×1020个 |