X、Y、Z、W、U是分别位于短周期的元素,原子序数依次递增。X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13。Y元素的单质在X的某种氧化物中可燃。下列说法正确的是
| A.W的最高价氧化物能与水反应生成相应的酸 |
| B.Y、Z元素的单质作电极,在NaOH溶液下构成原电池,Z电极上产生大量气泡 |
| C.室温下,0.05 mol/L U的气态氢化物的水溶液的pH>1 |
| D.Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
要检验某溴乙烷中的溴元素,正确的实验方法是( )
| A.加入溴水振荡,观察水层是否有棕红色出现 |
| B.滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无浅黄色沉淀生成 |
| C.加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
| D.加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
有机物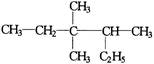 的正确命名为()
的正确命名为()
| A.2-乙基-3,3-二甲基-4-乙基戊烷 | B.3,3-二甲基-4-乙基戊烷 |
| C.3,3,4-三甲基已烷 | D.2,3,3-三甲基已烷 |
写出下列元素原子的电子排布式
P,Cr,
Al,Cu,
下列叙述中正确的是( )
A.BF3、H2O和NH3都是极性分子
B CO2和 C2H4都是含有极性键的非极性分子
C.HF、HCl、HBr、HI稳定性依次增强
D.NH3、SiH4、SO3都是四面体型分子
主族元素X和Y ,Xm-和Yn+核外电子排布相同,下列说法正确的为( )
| A.X的原子半径大于Y | B.X和Y的核电荷数之差为m-n |
| C.电负性X>Y | D.第一电离能X<Y |