下列实验方案中,能达到实验目的的是
| 选项 |
实验目的 |
实验方案 |
| A |
证明非金属性S>C |
向碳酸氢钠溶液中加入盐酸,观察是否有气泡冒出 |
| B |
比较HClO 和CH COOH 的酸性强弱 |
室温下,用pH 试纸分别测定浓度为0.1mol·L-1NaClO 溶液和0.1mol·L-1CH COONa 溶液的pH |
| C |
证明Na2 CO3溶液中存在水解平衡 |
向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 |
| D |
证明在相同温度下的Ksp: Mg(OH)2>Fe(OH)3 |
向10mL0.2mol·L-1NaOH溶液加入2滴0.1mol·L-1MgCl2溶液,产生白色沉淀后,再滴加2 滴0.1 mol/LFeCl3溶液,又生成红褐色沉淀 |
下列有关物质浓度关系的描述中,正确的是
| A.25℃时,向0.1mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42—)>c(OH—)=c(H+) |
| B.25℃时,NaB溶液的pH=8,c(Na+) + c(B-)=9.9×10-7mol·L-1 |
| C.0.1mol·L-1的NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| D.同温下,pH相同时,溶液物质的量浓度:c(CH3COONa)<c(NaHCO3)<c(C6H5ONa)<c(Na2CO3) |
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
取等物质的量的两种金属单质X、Y,分别与足量的盐酸反应 |
X产生氢气的体积比Y多 |
金属性:X>Y |
| B |
等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 |
HA放出的氢气多且反应速率快 |
HA酸性比HB强 |
| C |
在CuSO4溶液中加入KI溶液,再加入苯,振荡 |
有白色沉淀生成,苯层呈紫色 |
白色沉淀可能为CuI |
| D |
取久置的Na2O2粉末,向其中滴加过量的盐酸 |
产生无色气体 |
Na2O2没有变质 |
依曲替酯是一种皮肤病用药,它可以由原料X经过多步反应合成。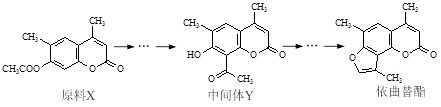
下列说法正确的是
| A.原料X与中间体Y互为同分异构体 |
| B.原料X可以使酸性KMnO4溶液褪色 |
| C.中间体Y能发生加成、取代、消去反应 |
| D.1 mol依曲替酯只能与1 mol NaOH发生反应 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是
| A.原子半径:rW>rZ>rY>rX |
| B.含Y元素的盐溶液有的显酸性,有的显碱性 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.X与氢元素组成的化合物XH5与水反应可产生两种气体 |
下列说法中正确的是
| A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g);ΔH<0,则该反应一定能自发进行 |
| B.提取海带中碘元素时,为将I-完全氧化为I2,用HNO3作氧化剂比用H2O2效果好 |
| C.原电池放电过程中,负极质量一定减轻,正极的质量一定增加 |
| D.由于Ksp(MgCO3)<Ksp[Mg(OH)2],因此水垢中MgCO3会逐渐转化为Mg(OH)2 |