若A + 酸 = 盐 + 水,则A不可能属于
| A.氧化物 | B.单质 | C.碱 | D.电解质 |
共价键、离子键、配位键和范德华力是粒子之间的四种作用力。现有下列晶体:①Na2O2②SiO2③[Cu(NH3 )4]Cl2④NH4Cl ⑤ NaCl ⑥ AlCl3,其中含有三种作用力的是()
| A.只有①②③ | B.只有①②③⑥ | C.只有③④⑥ | D.只有③④ |
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是()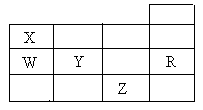
| A.常压下五种元素的单质中,Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的沸点比X的氢化物的沸点高 |
| D.Y元素的非金属性比W元素的非金属性强 |
下列各组原子中,彼此化学性质一定相似的是()
| A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
| C.2p轨道上有三个未成对的电子的X原子与3p轨道上有三个未成对的电子的Y原子 |
| D.最外层都只有一个电子的X、Y原子 |
下列叙述中正确的是()
| A.NH3、CO、CO2都是极性分子 |
| B.CH4、CCl4都是含有极性键的非极性分子 |
| C.HF、HCl、HBr、HI的稳定性依次增强 |
| D.CS2、H2O、C2H2都是直线型分子 |
现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是()
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③>②>① | D.最高正化合价:③>②>① |