100mL、0.5mol/L的(NH4)2SO4溶液中含有NH4+ mol,这些NH4+中所含有的电子数为 ,质子数为 。
下列物质中互为同分异构体的有 ,互为同素异形体的有 ,属于同位素的有 ,属于同一种物质的有 。(填序号)
①液氯 ②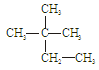 ③白磷 ④18O ⑤
③白磷 ④18O ⑤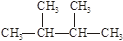
⑥红磷⑦16O⑧氯气
有机高分子化合物在日常生活中有非常广泛的应用。一种广泛应用于电器、工业交通的工程塑料DAP的结构简式是: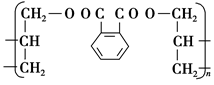
试回答:
(1)生产DAP工程塑料的单体的结构简式是__________________________。
(2)DAP工程塑料的单体,可以由两种有机物通过一步反应合成出来,则这两种有机物的结构简式是____________________和_______________。
合成有机玻璃的反应方程式如下: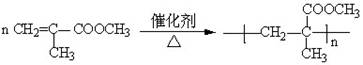
化学反应类型为______________________反应(填“加成聚合”或“缩合聚合”),其中单体是____________________,高分子化合物的链节为__________________,n值成为_______________,有机玻璃属于____________(填“纯净物”或“混合物”),原因是____________________________。
(1)已知某有机物的结构简式为: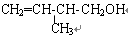 ,该有机物中所含官能团的名称是_______________________________,写出该有机物属于酮的同分异构体_______________(用结构简式表示)。
,该有机物中所含官能团的名称是_______________________________,写出该有机物属于酮的同分异构体_______________(用结构简式表示)。
(2)已知某高分子化合物的结构简式为: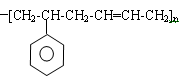 ,写出合成该高分子化合物的单体_______________(用结构简式表示)。
,写出合成该高分子化合物的单体_______________(用结构简式表示)。
根据下图所示化合物的结构,分析回答下列问题。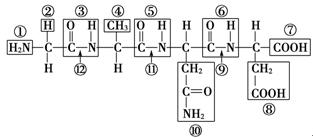
(1)该化合物中,①表示________,②表示________。
(2)该化合物由________个氨基酸失去________个水分子而形成。
(3)该化合物称为________,含________个肽键,编号是________________。