在25℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbL NaOH溶液,(题中a≤b,b≥8)。问:
(1)若a+b=14,则Va/Vb= .
(2)若a+b=13,则Va/Vb=
(3)若a+b>14,则Va/Vb= ,且Va Vb(填“>”“<”“=”)
用图示装置制取少量乙酸乙酯(酒精灯、铁架台等在图中均已略去),请填空: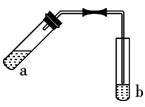
(1)写出试管a中发生反应的化学方程式
(2)某同学在实验过程中,试管a中忘记加入碎瓷片就加热进行实验,为防止暴沸,下一步的操作是:。
(3)实验中加热试管a的目的是:
①:
②:
(4)反应结束后,振荡试管b静置,观察到的现象是
。
23.(10分)下表是某超市出售的加碘食盐的有关说明:
| 精制盐、碘酸钾 |
|
| 含碘量 |
45±5mg/kg |
| 储藏方法 |
通风、防潮 |
| 食用方法 |
根据烹调所需适量加入 |
某研究性学习小组欲通过实验检验该碘盐中是否含碘:
(1)首先取该食盐样品配制室温下的饱和溶液:向200 mL蒸馏水中加入75.0g该食盐样品,加热并搅拌,直到完全溶解。冷却至室温。(已知室温条件下氯化钠溶解度为36 g)
在加热过程中需要用到的仪器有铁架台、酒精灯、铁圈、____________、烧杯和玻璃棒。冷却至室温过程中若出现____________________(填现象),则证明其为饱和溶液。
(2)甲同学先向该饱和食盐溶液中加入1mol/L的KI溶液和几滴淀粉溶液,然后加入0.1mol/L稀硫酸,振荡,溶液变为蓝色。该实验发生的化学反应中氧化剂与还原剂的物质的量之比为_______________。请在下图中画出参加反应的IO3—的物质的量和析出的I2单质的物质的量的关系曲线。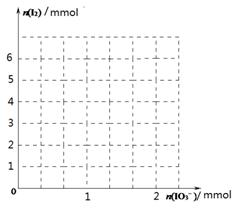
(3)乙同学认为甲同学的实验方案不严谨,他提出如下假设:空气中的氧气可能参与反应,使溶液变蓝。反应的离子方程式为:_____________________________________。
请你设计实验方案验证乙同学的假设是否正确:
。
某实验小组分别用图1、2装置测定某种钙片中碳酸钙的含量,夹持装置已略去。
提供的试剂:研细的钙片粉末(钙片中的其他成分不与盐酸反应)、2mol/L 盐酸、5%NaOH溶液、饱和Na2CO3溶液、饱和NaHCO3溶液和蒸馏水。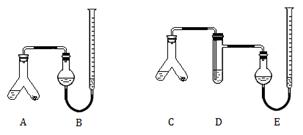
图1图2
实验过程:
I.检查两套装置的气密性。
II.在A、C的右边加入0.25 g钙片粉末,左边加入3 mL 2mol/L盐酸,塞紧塞子。在B、E中均加入饱和NaHCO3溶液,如图所示,记下量气管读数。
Ⅲ.将A、C倾斜,使液体与固体混合,实验结束并冷却后读出量气管读数,测得 B中收集到的气体为41.90 mL,E中收集到的气体体积为39.20 mL(以上气体体积均已折算为标准状况下的体积)。
回答下列问题:
(1)I中检查图1装置气密性的方法是。
(2)A中发生反应的离子方程式为;D中加入的试剂为。
(3)实验前左右两管液面在同一水平面上,最后读数时右管的液面高于左管的液面,
应进行的操作是。
(4)图2实验所得钙片中的碳酸钙的质量分数为;图1实验比图2实验所得钙片中的碳酸钙含量偏高,用离子方程式表示偏高的原因:。
实验室需要用0.1mol/LNaOH溶液450mL,根据溶液配制和使用回答下列问题:
(1)实验中除了托盘天平、烧杯、容量瓶外还需要的其它仪器有:
。
(2)根据计算得知,所需称量的NaOH的质量为g。
(3)下列操作对所配浓度有何影响(填写字母)偏大的有。
| A.称量用了生锈的砝码 |
| B.将NaOH放在纸张上称量 |
| C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中 |
| D.往容量瓶转移时,有少量液体溅出 |
E.未洗涤溶解NaOH的烧杯
F.定容时俯视刻度线
G.容量瓶未干燥即用来配制溶液
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
(共10分)如图,在试管a中先加入2mL95%的乙醇,边摇动边缓缓加入5mL浓H2SO4并充分摇匀,冷却后再加入2g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
(1)写出a试管中的主要化学反应的方程式;
(2)加入浓H2SO4的目的是。
(3)试管b中观察到的现象是。
(4)在实验中球形干燥管除起冷凝作用外,另一个重要作用是。
(5)饱和Na2CO3溶液的作用是。