下列陈述Ⅰ、Ⅱ都正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
浓硫酸有强氧化性 |
浓硫酸不能用于干燥H2S和HI气体 |
| B |
NH4Cl为强酸弱碱盐 |
用加热法除去NaCl中的NH4Cl |
| C |
溶解度:CaCO3<Ca(HCO3)2 |
溶解度:Na2CO3<NaHCO3 |
| D |
SiO2是两性氧化物 |
SiO2能与NaOH溶液和氢氟酸反应 |
下列变化属于化学变化的是
| A.碘的升华 | B.碘化银用于人工降雨 |
| C.液溴的气化 | D.漂白粉久置失效 |
19世纪中叶,门捷列夫的突出贡献是
| A.提出原子学说 | B.发现元素周期律 |
| C.提出分子学说 | D.发现氧气 |
下列实验能获得成功的是(填序号)
①将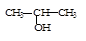 与NaOH的醇溶液共热制备CH3—CH=CH2
与NaOH的醇溶液共热制备CH3—CH=CH2
②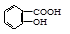 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备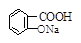
③检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,加入银氨溶液析出银镜
④用溴水即可检验CH2=CH-CHO中的碳碳双键
⑤将1-氯丙烷与NaOH溶液共热几分钟后,冷却、加入过量稀硝酸酸化,滴加AgNO3溶液,得白色沉淀,证明其中含有氯元素
⑥向浓苯酚中加几滴稀溴水观察到沉淀
⑦取2mL 1mol·L-1CuSO4溶液于试管中,加入1mL 2mol·L-1NaOH溶液,在所得混合物中加入40%的乙醛溶液,加热得到砖红色沉淀
⑧将乙醛滴入银氨溶液中,加热煮沸制银镜
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是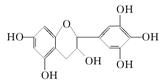
①分子式为C15H14O7
②1 mol儿茶素A在一定条件下最多能与7 mol H2加成
③等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1∶1
④1 mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4 mol
| A.①② | B.②③ | C.③④ | D.①④ |
丙烷的分子结构可简写成键线式结构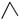 ,有机物A的键线式结构为
,有机物A的键线式结构为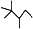 ,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是
,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是
A.有机物A的一氯取代物只有4种
B.用系统命名法命名有机物A,名称为2,2,3—三甲基戊烷
C.有机物A的分子式为C8H18
D.B的结构可能有3种,其中一种名称为3,4,4—三甲基—2—戊烯