下列各组烃的混合物,只要总质量一定,按任意比例混合,完全燃烧后生成的CO2和H2O都是恒量的是
| A.C2H2、C2H4 | B.C2H4、C4H6 |
| C.C2H6、C3H6 | D.C6H6、C2H2 |
下列分子的空间构型可用sp3杂化轨道来解释的是
①PCl3 ②CH2===CH2 ③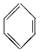 ④CH≡CH ⑤NH3 ⑥CH4
④CH≡CH ⑤NH3 ⑥CH4
| A.①②③ | B.①⑤⑥ | C.②③④ | D.③⑤⑥ |
X元素的价电子结构为ndn+2(n+1)sn-2,则下列判断正确的是
| A.X元素的电子排布式为:1S22S22P63S23P63d104s24p64d65s2 |
| B.X元素位于第五周期 |
| C.X元素位于VIB族 |
| D.X元素原子最外层有2个电子 |
化学中很多“规律”都有其适用范围,据下列 “规律”推出的结论合理的是
| A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
| B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| C.根据价电子构型与元素位置的关系,推出价电子数为3的元素一定在第ⅢA族 |
| D.根据较强酸可以制较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
下列说法一定正确的是
| A.元素的性质呈周期性变化的根本原因是第一电离能呈周期性变化 |
| B.3p能级上只有一个空轨道的原子所对应的元素和3p能级上有一个未成对电子的原子所对应的元素属于同一周期 |
| C.电子层数少的元素的原子半径小于电子层数多的元素的原子半径 |
| D.键长短的共价键的键能大于键长长的共价键的键能 |
下列各项叙述中,说法不正确的是
| A.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 |
| B.镁原子由1s22s22p63s2→1s22s22p63p2时,原子吸收能量,由基态转化成激发态 |
| C.最外层电子排布为ns2np6(当只有K层时为1s2)的原子,第一电离能较大 |
| D.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |