已知Fe3O4可表示成(FeO·Fe2O3),水热法制备Fe3O4纳米颗粒的总反应为3Fe2++2S2O32-+O2+4OH- Fe3O4+S4O62-+2H2O。下列说法正确的是
Fe3O4+S4O62-+2H2O。下列说法正确的是
| A.O2是氧化剂,S2O32-和Fe2+是还原剂 |
| B.每生成1 mol Fe3O4,则转移电子数为2 mol |
| C.参加反应的氧化剂与还原剂的物质的量之比为1:2 |
| D.若有2 mol Fe2+被氧化,则被Fe2+还原的O2为0.5 mol |
下列叙述不能作为元素周期表中元素排列顺序依据的是
| A.原子的中子数 | B.原子的核电荷数 |
| C.原子的质子数 | D.原子的核外电子数 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是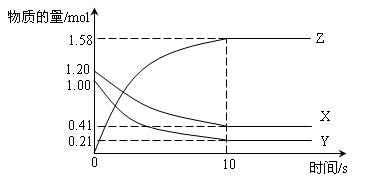
| A.反应开始到10s,用Z表示的反应速率为0.158 mol·L-1·s-1 |
| B.10s后,该反应停止进行 |
C.反应的化学方程式为:2X(g) + Y(g)  2Z(g) 2Z(g) |
| D.反应开始到10s时,平均反应速率:v(X)=" v(Y)=0.0395" mol·L-1·s-1 |
恒温恒容条件下可逆反应H2(g)+I2(g)  2HI(g)达到平衡时的标志是
2HI(g)达到平衡时的标志是
| A.H2、I2、HI的浓度均相等 | B.1个I-I键断裂的同时,有1个H-I键断裂 |
| C.混合气体的质量不再改变 | D.混合气体的颜色不再改变 |
分子式C4H=O2的有机物与稀硫酸溶液共热可得有机物A和B。将A氧化最终可得C,且B和C为同系物。若C可发生银镜反应,则原有机物的结构简式为()
A.HCOOCH2CH2CH3 B.CH3COOCH2CH3
C.CH3CH2COOCH3 D.HCOOCH(CH3)2
NA为阿伏加德罗常数,下列说法正确的是()
| A.标准状况下,11.2的甘油所含的分子数为0.5NA |
| B.28g乙烯所含共用电子对数目为4NA |
| C.1.6g甲烷所含电子数为0.5NA |
| D.14g丙烯所含原子数为3NA |