Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。Q元素的原子最外层电子数是其内层电子数的2倍。W、Z最外层电子数相同,Z的核电荷数是W的2倍。元素Y的合金是日常生活中使用最广泛的金属材料之一,下列说法正确的是
| A.原子半径的大小顺序:rY> rX >rQ>rW |
| B.X、Y的最高价氧化物的水化物之间不能发生反应 |
| C.Z元素的氢化物稳定性大于W元素的氢化物稳定性 |
| D.元素Q和Z能形成QZ2型的共价化合物 |
复合材料的使用使导弹的射程有了很大的提高,其主要原因是( )
| A.复合材料的使用可以使导弹经受超高温的变化 |
| B.复合材料的使用可以使导弹的质量减轻 |
| C.复合材料的使用可以使导弹承受温度的剧烈变化 |
| D.复合材料的使用可以使导弹承受超高强度的变化 |
维通橡胶是一种耐腐蚀、耐油、耐高温、耐
寒性能都特别好的氟橡胶。它的结构简式见右图: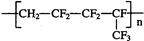 合成它的单体为
合成它的单体为
| A.氟乙烯和全氟异丙烯 | B.1,1-二氟乙烯和全氟丙烯 |
| C.1-三氟甲基-1,3-丁二烯 | D.全氟异戊二烯 |
载人飞船,飞船冲破大气层摆脱地球吸引力,高速运行时会与大气发生摩擦,普通金属材料如钛合金、铝合金摩擦一段时间就会燃烧,因此需要在“神舟七号”的表面涂一层吸热 快、能自动脱落的复合陶瓷,对这种复合陶瓷描述正确的是 ( )
| A.这种复合陶瓷是传统的硅酸盐产品 |
| B.这种复合陶瓷具有耐高温特性、光学特性、生物特性 |
| C.这种陶瓷虽然克服了传统无机非金属材料的缺点,但强度较差 |
| D.这种复合陶瓷具有耐高温、隔热、耐摩擦、硬度大等特点 |
神舟七号返回舱约3吨多重,是世界上现有的最大的返回舱。为了防止飞船与大气摩擦产生高温而起火燃烧,在飞船表面覆盖着某种特殊材料,该材料应具有的性质是()
| A.良好的导电性 |
| B.密度较大,以增大飞船对地面的惯性 |
| C.轻质防热,可以承受上千度的高温 |
| D.质地柔软,以利于飞船变形 |
下列关于金属的腐蚀叙述正确的是
| A.金属在潮湿的空气中腐蚀的实质是M+nH2O=M(OH)n+n/2H2↑ |
| B.金属的化学腐蚀实质是M→Mn+ +ne-,电子直接转移给氧化剂 |
| C.金属的化学腐蚀必须在酸性条件下进行 |
| D.在潮湿的中性环境中,金属的电化学腐蚀主要是析氢腐蚀 |