(7分)工业尾气SO2、NO2是污染大气、形成酸雨的罪魁祸首。请回答下列问题:
(1)用CO可以消除SO2污染。已知一定条件下,2CO(g)+O2(g)==2CO2(g)的能量变化如图所示,由固体S单质生成l molSO2(g)的焓变为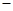 296kJ·mol
296kJ·mol 。
。
在相同条件下,CO与SO2反应生成单质S与CO2的热化学方程式为___________________________。
(2)异氰酸(化学式:HNCO,C为+4价)可用于消除尾气中的NO2。其反应原理为:
HNCO+NO2→N2+CO2+ (未配平)。
(未配平)。
①上述反应的氧化剂是____________。
②配平后方框内应填写____________。
③每处理33.6LNO2(标准状况),反应中转移电子的物质的量为____________。
下列有机化合物中,有多个官能团: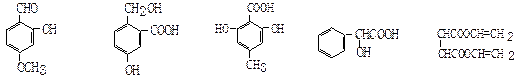
| A. | B. | C. | D.E. |
⑴可以看作醇类的是(填入编号,下同):_____________;
⑵可以看作酚类的是________;
⑶可以看作羧酸类的是__________________;
⑷可以看作酯类的是____________。
把除去氧化膜的镁条投入到盛有少量稀盐酸的试管中,发现氢气发生的速率变化情况如图所示。其中t1—t2速率变化的主要原因是______________________________;t2—t3速率变化的主要原因是________________________________________。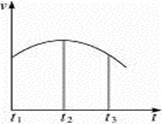
有铜片、锌片和250mL稀硫酸组成的原电池,当在铜片上放出4.48L(标准状况下)的气体时,硫酸恰好完全反应。
(1)该原电池的负极反应式
(2) 原稀硫酸的物质的量浓度是mol/ L
(3)锌片减少的质量
下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ___ ___,⑥ ______,⑦ __ __。
(2)画出原子的结构示意图:④___ __ ___,⑧___。
(3)在①~12元素中,金属性最强的元素是_____,非金属性最强的元素是___ ___,最不活泼的元素是____。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是(填序号),跟它同周期原子半径最小的元素是(填序号),它们可以形成(填离子或共价)化合物,用电子式表示其形成过程如下:。
在14 6C、14 7N、16 8O、3517CL、235 92U、238 92U中;
(1)____________和_____________互为同位素;
(2)___________和______________的质量数相等,但不能互称为同位素;
(3)___________和______________的中子数相等,但质子数不相等,所以不是同一种元素;
(4)以上所列共有_____________种元素;