下列有关胶体的说法正确的是
| A.分散质粒子直径介于10-9 m~10-7m之间的分散系称为胶体 |
| B.电泳现象可证明胶体带有电荷 |
| C.用聚光手电筒照射FeCl3溶液和Fe(OH)3胶体时,产生的现象相同 |
| D.Fe(OH)3难溶于水,因此可以用向煮沸的氢氧化钠溶液中滴加饱和三氯化铁溶液的方法制备氢氧化铁胶体。 |
如图所示是四种常见有机物的比例模型示意图。下列说法正确的是
| A.22.4 L甲中含有10 mol电子 |
| B.乙与乙的加聚产物都能使溴水褪色 |
| C.丙不能与溴水、酸性高锰酸钾溶液发生反应 |
| D.丙、丁都可以萃取溴水中的溴单质 |
某二元酸H2A的电离方程式为:H2A=H++HA-;HA- A2-+ H+。下列说法正确的是
A2-+ H+。下列说法正确的是
A.Na2A溶液中:c(Na+)>c(A2-)>c (HA-)>c(H2A)
B.NaHA溶液中:c(Na+)=c(A2-)+c(HA-)
C.Na2A溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A)
D.室温下0.1mol/L的H2A溶液pH大于1
某研究小组利用电化学方法处理石油炼制过程中产生的含H2S的废气。基本工艺是将H2S通入FeCl3溶液中,过滤后将滤液加入电解槽中电解,如图所示,下列有关说法正确的是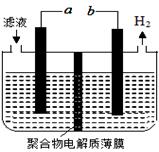
| A.过滤得到的沉淀可能是FeS |
| B.与a极相连的电极反应式为2Cl--2e-=Cl2 |
| C.可以用Fe与外接电源的a极相连 |
| D.电解后的滤液可以循环利用 |
已知乙醇、石墨和氢气的燃烧热分别为a、b、c (均为正值,单位均为kJ·mol-1 )。则反应2C(石墨,s)+2H2(g)+H2O(l)=C2H5OH(l)的焓变为
| A.(2b+2c-a)kJ·mol-1 | B.(a-2b-2c) kJ·mol-1 |
| C.(b+c-a) kJ·mol-1 | D.(a-2b-c) kJ·mol-1 |
W、X、Y、Z为原子序数递增的四种短周期元素。W是原子半径最小的元素,X的一种核素在考古时常用来鉴定一些文物的年代,Y是植物生长所需化学肥料中主要的营养元素之一,Z原子的最外层电子数是X原子最外层电子数的1.5倍。下列说法正确的是
| A.氢化物的沸点:Z一定高于Y |
| B.最高价氧化物对应水化物的酸性:X强于Y |
| C.W、X、Y、Z都能分别与氯元素形成共价化合物 |
| D.仅由W、Y、Z三种元素组成的化合物不可能属于盐类 |