VL Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量的浓度为
A. mol/L mol/L |
B.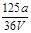 mol/L mol/L |
C.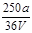 mol/L mol/L |
D.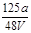 mol/L mol/L |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族,X+与M2-具有相同的电子层结构,离子半径:Z2->W-,Y的单质晶 体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
| A.X、M两种元素只能形成X2M型化合物 |
B.由于W、Z、M元素的氢化物相对分子质量 依次减小,所以其沸点依次降低 依次减小,所以其沸点依次降低 |
| C.元素Y在自然界中主要以单质形式存在 |
| D.元素W的单质可作为水处理中的消毒剂 |
下列说法正确的是
| A.二氧化碳能与水反应生成相应的酸,二氧化硅也能与水反应生成相应的酸 |
| B.D216O中,质量数之和是质子数之和的两倍 |
| C.氯化氢的沸点比氟化氢的高 |
| D.第ⅠA族的元素形成的氧化物均为碱性氧化物 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性:W>Z |
| C.Z的单质与氢气反应较Y的单质与氢气反应剧烈 |
| D.X、Y形成的化合物都易溶于水 |
门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是
| A.X单质不易与水反应 | B.XO2可被碳或氢气还原为X |
C.XCl4的沸点比SiCl4的高 |
D.XH4比SiH4稳定 |
下列实验中,不能观察到明显变化的是
| A.把一段打磨过的镁带放入冷水中 |
| B.把Cl2通入FeCl2溶液中 |
| C.把绿豆大的钾投入水中 |
| D.把溴水滴加到KI淀粉溶液中 |