下表中评价合理的是
| 选项 |
化学反应及其离子方程式 |
评价 |
| A |
铁与稀盐酸反应: 2Fe+6H+=2Fe3++3H2↑ |
正确 |
| B |
大理石溶于醋酸的反应: CaCO3+2H+=Ca2++CO2↑+H2O |
错误,醋酸应写为分子形式CH3COOH,CaCO3应写成离子形式 |
| C |
向Ba(OH)2溶液中滴加少量NaHCO3溶液:Ba2+ + OH- +HCO3- = BaCO3↓+ H2O |
错误,方程式中Ba2+和OH-化学计量数之比为1:2 |
| D |
NH4HCO3溶液与过量KOH浓溶液共热: NH4++ OH-  NH3↑+ H2O NH3↑+ H2O |
错误,HCO3-也可以与OH-反应 |
T℃时,在2L的密闭容器中,气体X、Y和Z三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是
| A.容器中化学反应为X(g)+Y(g)=Z(g) |
| B.0~10s,X表示的平均化学反应速率为0.04mol/(L·S) |
| C.使用催化剂只能加快0~10 s间的反应速度 |
| D.0~4 s的平均反应速率小于0~10s时平均反应速率 |
元素氟位于周期表右上角,下列对元素氟的相关叙述正确的是
| A.还原性:F— > Br— | B.酸性:HF>HCl |
| C.半径:F<Cl | D.稳定性:HF < HCl |
《读卖新闻》3月25日:日本东京电力公司24日宣布,在对福岛第一核电站排水口的海水进行取样化验后,检测出含有微量的放射性物质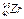 。专家表示,这些放射物质来自于核燃料棒。锆被发现了,说明堆心已经彻底熔毁;这不是几年就能解决的问题,最坏的情况发生了。日本前景堪忧!下列关于
。专家表示,这些放射物质来自于核燃料棒。锆被发现了,说明堆心已经彻底熔毁;这不是几年就能解决的问题,最坏的情况发生了。日本前景堪忧!下列关于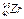 的说法正确的是
的说法正确的是
A.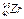 和 和 两原子的核外电子总数相等 两原子的核外电子总数相等 |
B.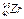 的中子数和电子数之差为55 的中子数和电子数之差为55 |
C.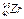 和 和 是同种核素 是同种核素 |
D.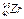 属于非金属元素 属于非金属元素 |
下列说法正确的是
A.需要加热才能发生的反应 一定是吸热反应 一定是吸热反应 |
| B.任何放热反应在常温条件下一定能发生反应 |
| C.吸热反应必须在高温才能发生 |
| D.反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
右图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。
挤压胶管的胶头,下列与试验事实不相符的是()
| A.CO2(NaHCO3溶液)无色喷泉 |
B.NH3(H2O含酚酞)红 色喷泉 色喷泉 |
| C.H2S(CuSO4溶液)黑色喷泉 |
| D.HCl(AgNO3溶液)白色喷泉 |