氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| D.氨气分子是极性分子而甲烷是非极性分子 |
化合物X、Y、Z之间有如图所示的转化关系。下列说法中不正确的是
| A.图中的每一步反应都是氧化还原反应 |
| B.钠与Y物质的反应属于氧化还原反应,但不是离子反应 |
| C.X与Y的反应中,氧化剂和还原剂都是X |
| D.Z的水溶液能使酚酞试液变红 |
下列说法正确的是
| A.已知CO(g)的燃烧热ΔH=-283.0 kJ·mol-1,则表示CO燃烧热的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ/mol |
| B.等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多。 |
| C.H2(g)+F2(g)=2HF(g);ΔH1="a" kJ/mol;H2(g)+Cl2(g)=2HCl(g);ΔH2="b" kJ/mol ΔH1<ΔH2 |
D.C(s)+H2O(g)  CO(g)+H2(g);ΔH>0,若平衡后再充入一定量水蒸气,则ΔH增大 CO(g)+H2(g);ΔH>0,若平衡后再充入一定量水蒸气,则ΔH增大 |
关于原子轨道的说法正确的是
| A.凡是中心原子采取sp3杂化轨道成键的分子立体构型都是正四面体 |
| B.CH4中的sp3杂化轨道是4个H原子的1s 轨道和C原子的2p轨道混合形成 |
| C.sp3杂化轨道是由同一原子中能量相近的s 和p轨道混合形成的一组新轨道 |
| D.凡AB3型的共价化合物,中心原子A均采用sp3杂化轨道成键 |
向下图所示的装置中缓慢地通入气体X,若关闭活塞K,则品红溶液无变化;若打开活塞K,则品红溶液褪色。X和Y可能是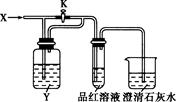
| A |
B |
C |
D |
|
| X |
SO2 |
NO2 |
HCl |
C12 |
| Y |
饱和NaHCO3溶液 |
水 |
Na2SO3溶液 |
Na2SO3溶液 |
两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n。下列说法错误的是
| A.若8>m>3,则X必定为主族元素 |
| B.若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y>X |
| C.若Y的气态氢化物化学式为YHn,且b<4,则该氢化物为非极性分子 |
| D.若a=b=3,8>m>n>b,则元素非金属性:X>Y |