“雾霾”已成为当今世界环境热点话题,为减少CO、SO2、NOx等气体的排放,某环境小组研究使用如下方式。
Ⅰ.使用清洁能,例如二甲醚( DME)。现由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1=—90.7KJ/mol
CH3OH(g) ΔH1=—90.7KJ/mol
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=—23.5KJ/mol
CH3OCH3(g)+H2O(g) ΔH2=—23.5KJ/mol
③CO(g)+ H2O(g) CO2(g)+H2(g) ΔH3=—41.2KJ/mol
CO2(g)+H2(g) ΔH3=—41.2KJ/mol
回答下列问题:
(1)则反应3CO(g)+3H2(g)  CH3OCH3(g)+ CO2(g) 的ΔH =______KJ/mol;
CH3OCH3(g)+ CO2(g) 的ΔH =______KJ/mol;
(2)将合成气以甲n(H2)/n(CO)=2通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g) CH3OCH3 (g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是 (填字母序号)。
CH3OCH3 (g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是 (填字母序号)。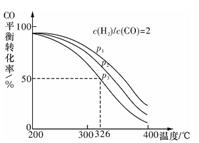
A.△H<O
B.P1< P2<p3
C.若在p3和316℃时,起始n(H2)/n( CO)= 3,则达到平衡时,CO的转化率小于50%
(3)如图为绿色“二甲醚燃料电池”的工作原理示意图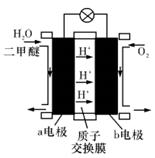
a电极的电极反应式为:
Ⅱ.利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通人4 mol CO,测得CO2的体积分数
5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通人4 mol CO,测得CO2的体积分数 (CO2)随时间t变化曲线如图。
(CO2)随时间t变化曲线如图。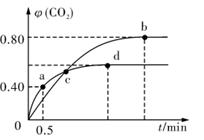
请回答:(1)从反应开始至a点时的反应速率为v(CO) 。
(2)b点时化学平衡常数Kb= 。
(3)下列说法不正确的是 (填字母序号)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.增大d点的体系压强,CO的转化率不变
D.b点和d点的化学平衡常数:Kb<Kd
(8分)现有CH4、C2H4、C2H6三种有机物:
(1)等质量的以上三种物质完全燃烧时耗去O2的量最多的是________;生成CO2量最多的是________。
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是________。
(3)在120 ℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是________。
(11分) A、B、C、D、E、F、G、H和I是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①A、B、E、F、G能使湿润的蓝色石蕊试纸变红,I能使湿润的红色石蕊试纸变蓝,C、D、H不能使湿润的石蕊试纸变色;
②A和I相遇产生白色的烟;
③B和E都能使品红溶液褪色;
④将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟;
⑤将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
⑥C和D相遇生成红棕色气体;
⑦G在D中燃烧可以产生E和H2O;
⑧将B和H在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生A。
回答下列问题:
(1)A的化学式是________,②中烟的化学式是________;
(2)④中发生反应的化学方程式是
________________________________________________________________________;
(3)⑤中发生反应的化学方程式是
________________________________________________________________________;
(4)C的化学式是__________,D的化学式是__________;
(5)⑦中发生反应的化学方程式是
________________________________________________________________________;
(6)H的化学式是________。
(14分)阅读讨论并完成以下各项内容:
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02 mg/L。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的SO2和氮的氧化物。它们的主要来源是煤和石油的燃烧,全世界每年排放1.5亿吨的SO2。
①SO2可在空气中受光照等因素作用而被氧化,最终与雨水形成硫酸型酸雨。试写出这两个化学反应的方程式
________________________________________________________________________;
________________________________________________________________________。
②汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107 kg。NO2溶于水生成 ________和NO。
③酸雨可导致的危害有________(填序号)。
A.腐蚀建筑物 B.导致树木枯萎
C.造成洪涝灾害 D.恶化人类环境
④为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫化物进行________,对废气中的氮的氧化物用________吸收。
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量(已知碘能氧化H2SO3,生成H2SO4)。
①若原料气从左向右流时,上述装置连接的顺序是:原料气→________(用字母和箭头表示)。
②装置②中发生反应的离子方程式为:
________________________________________________________________________;
当装置②中出现________现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是________。
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
直接排放含SO2,的烟气会形成胶雨,危害环境。利用钠碱循环法可脱除烟气中的SO2
(1)在钠碱循环法中,Na2 SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,
该反应的离子方程式是
(2)吸收液吸收SO2的过程中,pH随n(SO3²-):n(HSO3﹣变化关系如下表:
| n(SO3²--):n(HSO3﹣) |
91:9 |
1:1 |
9:91 |
| PH |
8.2 |
7.2 |
6.2 |
①上表判断NaHSO3溶液显 性,原因:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a、C(Na+)==2C(SO32-)+C(HSO3-)
b、C(Na+)> C(HSO3-)> C(SO32-)>C(H+)==C(OH-)
c、C(Na+)+ C(H+)="=" C(SO32-)+ C(HSO3-)+ C(OH-)
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按下图所示步骤进行操作。回答下列问题:
(1)起始滤液的pH7(填“大于”、“小于”或“等于”),其原因是(用方程式表达)
(2)试剂I的化学式为,
(3)③中发生反应的化学方程式为;