下列混合溶液中,各离子浓度的大小顺序正确的是
| A.10 mL0.1 mol·L-1NH4Cl溶液与5 mL0.2 mol·L-1NaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| B.10 mL0.1 mol·L-1氨水与10 mL0.1 mol·L-1盐酸混合,c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.10 mL0.1 mol/LCH3COOH溶液与10 mL0.2 mol/LNaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D.10 mL0.5 mol·L-1CH3COONa溶液与5 mL1 mol·L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
维生素C(Vitamin C)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如右图。下列有关说法中正确的是()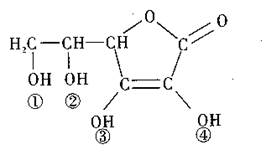 A.维生素C的分子式为C6H 16O6
A.维生素C的分子式为C6H 16O6
B.维生素C 由于含有酯基而难溶于水
C.维生素C由于含有C=O键而能发生
银镜反应
D.维生素C的酸眭可能是③、④两个
羟基引起的
用NA表示阿伏加德罗常数的值,下列说法正确的是()
| A.标准状况下,11.2LNO与5.6LO2混合后的分子总数为0.5NA |
| B.1mol癸烷所含共价键数为29NA |
| C.1mol乙烯基所含电子数为16NA |
| D.乙烯和环丙烷组成的28g混合气体中含有4NA个氢原子 |
将17.9 g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体3.36 L(标准状况)。另取等质量的合金溶于过量的稀硝酸中,生成6.72 LNO(标况),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为()
| A.33.2 g | B.25.4 g | C.22.4 g | D.19.6 g |
西维因是一种高效低毒杀虫剂,在碱性条件下可水解: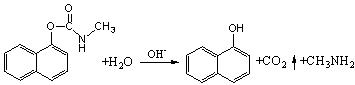
有关说法正确的是()
| A.西维因分子式为C12H10NO2 |
| B.反应后的溶液经酸化,可用FeCl3溶液检验西维因是否已经发生水解 |
| C.1mol西维因最多能与6mol氢气发生加成反应 |
| D.西维因分子中至少有21个原子共平面 |
根据化学平衡知识,判断下列说法正确的是()
A.已知NaHA溶液呈弱碱性,则该溶液中下列各种微粒浓度大小排列顺序为:
c(Na+)>c(HA-)>c(A2-)>c(H2A)
B.在小苏打溶液中存在下列关系:c(HCO3-)=c(Na+)-c (CO32-)-c(H2CO3)
C.向AgCl悬浊液中加入足量的NaI溶液,无明显现象产生
D.常温下,稀释0.1 mol/L的氨水,溶液中所有离子浓度均下降