已知碘蒸汽为紫红色,H2、HI均为无色气体。在一定温度和固定容积的密闭容器中进行的反应:H2 (g)+I2 (g)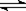 2HI(g),下列说法能充分说明该反应已达到化学平衡状态的是
2HI(g),下列说法能充分说明该反应已达到化学平衡状态的是
| A.H2、I2、HI的浓度相等 | B.容器内颜色不再改变 |
| C.H2、I2、HI在容器中共存 | D.正、逆反应速率均等于零 |
稀醋酸中CH3COOH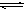 CH3COO-+H+已达平衡,若要使稀醋酸的电离度(弱电解质在溶液里达电离平衡时,已电离的电解质分子数占原来总分子数的百分数)和溶液的pH值都减小,应加入的试剂是
CH3COO-+H+已达平衡,若要使稀醋酸的电离度(弱电解质在溶液里达电离平衡时,已电离的电解质分子数占原来总分子数的百分数)和溶液的pH值都减小,应加入的试剂是
| A.CH3COONa | B.NH3·H2O | C.HCl | D.H2O |
在密闭容器中,对于可逆反应A+3B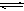 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
| A.若正反应方向ΔH<0,则T1>T2 |
| B.压强增大时,混合气体的平均相对分子质量减小 |
| C.B一定为气体 |
| D.A一定为气体 |
下列事实中,不能用勒夏特列原理解释的是
| A.对熟石灰的悬浊液加热,悬浊液中固体质量增加 |
| B.实验室中常用排饱和食盐水的方式收集氯气 |
| C.打开汽水瓶,有气泡从溶液中冒出 |
| D.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 |
反应2SO2(g)+O2(g)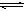 2SO3(g),经一段时间后SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.4mol·L-1·min-1,则这段时间为
2SO3(g),经一段时间后SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.4mol·L-1·min-1,则这段时间为
| A.0.5s | B.1s | C.30s | D.60s |
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)反应的
ΔH=-55.6 kJ·mol-1。则HCN在水溶液中电离的ΔH等于
| A.-67.7 kJ·mol-1 | B.-43.5 kJ·mol-1 |
| C.+43.5 kJ·mol-1 | D.+67.7 kJ·mol-1 |