将如图所示实验装置的K闭合,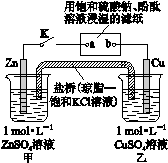
下列判断正确的是
| A.Cu电极上发生还原反应 |
| B.电子沿Zn→a→b→Cu路径流动 |
| C.片刻后甲池中c(SO42-)增大 |
| D.片刻后可观察到滤纸b点变红色 |
某化学兴趣小组在家中进行化学实验,按照图甲连接好线路发现灯泡不亮,按照图乙连接好线路发现灯泡亮。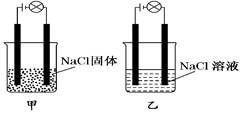
由此得出的结论正确的是
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl是弱电解质 |
| D.NaCl在水溶液中电离出了可以自由移动的离子 |
著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+,则下列说法中正确的是
| A.铈的冶炼方法为:用稀土串级萃取法对矿石进行萃取富集;然后电解熔融的CeO2 |
| B.CeO2溶于氢碘酸的化学方程式可表示为:CeO2+4HI=CeI4+2 H2O |
| C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+ |
| D.四种稳定的核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同位素 |
某同学设计如下实验测量m g铜 银合金样品中铜的质量分数:
银合金样品中铜的质量分数: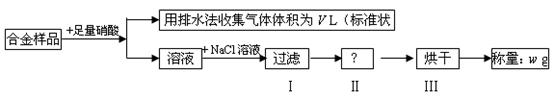
下列说法中不正确的是
| A.收集到的V L气体为 NO、NO2 |
| B.过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒 |
| C.操作Ⅱ应是洗涤 |
D.铜的质量分数为: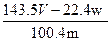 ×100% ×100% |
下列化学实验事实及其结论都正确的是
A.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝熔点高于铝
B.将SO2通入含HClO的溶液中,生成H2SO4,说明HClO酸性比H2SO4强
C .FeCl3溶液可以腐蚀线路板上的Cu,说明Fe的金属活动性大于Cu
.FeCl3溶液可以腐蚀线路板上的Cu,说明Fe的金属活动性大于Cu
D.将饱和氯水滴到淀粉碘化钾试纸上,试纸先变蓝后变白,说明氯水具有漂白性
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列分析中正确的是
| A.白色沉淀是CuI2,棕色溶液含有I2[ |
| B.滴加KI溶液时,转移1mole-时生成1mol白色沉淀 |
| C.通入SO2时,SO2与I2反应,I2作还原剂 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |