下列表述正确的是
A.NaH中氢离子结构示意图为: |
B.NH4I的电子式: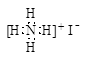 |
C.质子数是82,中子数是122的铅原子: Pb Pb |
D.CO2的比例模型: |
下列溶液无色,在pH=1时能大量共存的是
| A.CuSO4 NaCl KNO3 | B.NaOH NaCl NaNO3 |
| C.Na2SO4 NH4Cl ZnCl2 | D.K2SO4 AgNO3 NaCl |
将a、b、c三种金属分别投入稀盐酸中,只有b溶解并产生气泡;把a和c分别放入硫酸铜溶液中,在a表面有铜析出,c没有变化。则a、b、c的金属活动性顺序是
| A.c>b>a | B.b>a>c | C.a>c>b | D.b>c>a |
粗 盐中含可溶性 CaCl2、MgCl2 及一些硫酸盐,除去这些杂质的试剂可选用① Na2CO3
盐中含可溶性 CaCl2、MgCl2 及一些硫酸盐,除去这些杂质的试剂可选用① Na2CO3
② NaOH ③ BaCl2④ HCl,加入的先后顺序可以是
| A.①②③④ | B.②③①④ | C.②①③④ | D.①③②④ |
可以用来判定碳酸氢钠粉末中混有碳酸钠的实验方法是
| A.加热时有无色气体放出 |
| B.滴加盐酸时有气泡放出 |
| C.溶于水后,滴加稀的氯化镁溶液有白色沉淀生成 |
| D.溶于水后,滴加澄清石灰水有白色沉淀生成 |
下列关于钠的氧化物的叙述正确的是
| A.Na2O2是白色固体,和冷水作用得到O2和NaOH |
| B.Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水 |
| C.Na2O不稳定,能继续被O2氧化生成Na2O2 |
| D.都能与酸反应,生成含氧酸盐,都是碱性氧化物 |