某无色透明溶液中,下列离子能够大量共存的是
| A.H+、NH4+、AlO2-、S2O32- |
| B.K+、Cu2+、OH-、Cr2O72- |
| C.Na+、Al3+、SO42-、NO3- |
| D.Ag+、Mg2+、CO32-、I- |
分子式为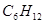 ,分子结构中含有3个“—
,分子结构中含有3个“—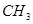 ”原子团的烯烃共有()
”原子团的烯烃共有()
| A.2种 | B.3种 | C.4种 | D.5种 |
下列离子或分子组中能大量共存,且满足相应要求的是()
| 选项 |
离子 |
要求 |
| A |
K+、NO3-、Cl-、HS- |
c(K+)<c(Cl-) |
| B |
Fe3+、NO3-、SO32-、Cl- |
逐滴滴加盐酸立即有气体产生 |
| C |
Na+、HCO3-、Mg2+、SO42- |
逐滴滴加氨水立即有沉淀产生 |
| D |
NH4+、Al3+、SO42-、CH3COOH |
滴加NaOH浓溶液立刻有气体产生 |
设NA为阿伏加德罗常数的值,下列叙述不正确的是()
| A.常温常压下,17 g甲基(—14CH3)所含的中子数为8 NA |
| B.室温下,31.0g白磷中含有的共价键数目为1.5NA |
| C.标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA |
| D.1 molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
化学与环境、材料、信息、能源关系密切,下列说法错误的是
| A.利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
| B.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| C.同时改变两个变量来研究反应速率的变化,不一定能更快得出有关规律 |
| D.防止酸雨发生的重要措施之一是使用清洁能源 |
下列有关溶液中微粒浓度关系的叙述正确的是
| A.向0.1 mol·L-1NH4Cl溶液中通入一定量氨气后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(C1O-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C.向CH3COONa溶液中滴加稀HCl至中性,所得溶液中:c(Cl-)>c(Na+)>c(CH3COOH) |
| D.等物质的量浓度CH3COOH溶液和CH3COONa溶液等体积混合,所得溶液中:c(CH3COOH)+2c(OH-)=2c(H+)+c(CH3COO-) |