标准状况下,VL氨气溶解在1L水中(水的密度近似为1g/ cm3),所得溶液的密度为ρ g/cm3,质量分数为ω,物质浓度为c mol/L。下列判断不正确的是
| A.溶液的浓度为c="Vρ/(17V+22400)" |
| B.用水稀释该溶液,OH-的物质的量增加 |
| C.该溶液中共有6种微粒 |
| D.上述溶液中再加入与该溶液体积相等的水后,所得溶液溶质的质量分数小于0.5ω |
已知某土壤胶体带负电荷,下列化肥在使用时,其肥效流失最为严重的是
| A.NH4Cl | B.(NH4)2SO4 | C.NH4HCO3 | D.NH4NO3 |
氮化硅陶瓷是一种超硬而且耐磨的物质,可用于制造高性能柴油机部件,它属于
| A.金属材料 | B.无机非金属材料 |
| C.复合材料 | D.功能高分子材料 |
维通橡胶是一种耐腐蚀、耐油、耐高温、耐寒性能都较好的氟橡胶。它的结构简式为: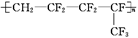 合成它的单体为
合成它的单体为
| A.氟乙烯和全氟异丙烯 | B.1,1-二氟乙烯和全氟丙烯 |
| C.1-三氟甲基-1,3-丁二烯 | D.全氟异戊二烯 |
心酮胺是治疗冠心病的药物。它具有如下的结构简式:下列关于心酮胺的描述,错误的是: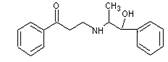
| A.可以在催化剂作用下和溴反应 | B.可以和银氨溶液发生银镜反应 |
| C.可以和氢气发生加成反应 | D.可以和浓硫酸与浓硝酸的混合液反应 |
玉米秸秆往往被当着燃料、饲料和有机肥使用,其实玉米秸秆可以在一定条件下水解生成葡萄糖,有着更高的经济价值,其实验包括下列一些操作步骤,正确的排列顺序是
①取少许玉米秸秆粉碎 ②小火微热,使之成为溶液 ③加90%的浓硫酸,用玻璃棒把秸秆粉末捣成糊④稍冷,滴入几滴硫酸铜溶液,并加入过量的NaOH溶液中和至出现氢氧化铜沉淀 ⑤加热煮沸
| A.①②③④⑤ | B.①③②④⑤ | C.①③②⑤④ | D.①②③⑤④ |