关于丙烯醇(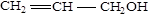 )的叙述不正确的是
)的叙述不正确的是
| A.可使酸性高锰酸钾褪色,反应类型为氧化反应 |
| B.一定条件下可与氢气反应生成丙醇,反应类型为加成反应 |
| C.一定条件下能与乙酸反应生成酯,反应类型为酯化反应 |
| D.该物质与乙醇属于同系物 |
将4molA(g)和2molB(g)在2L的恒容密闭容器中混合并在一定条件下发生如下反应::2A(g)+B(g) 2C(g),△H<0;反应2s后测得C的浓度为0.6mol/L.下列说法中正确的是
2C(g),△H<0;反应2s后测得C的浓度为0.6mol/L.下列说法中正确的是
A.2s后物质A的转化率为70%
B.达到平衡状态时,升高温度,则该化学平衡向左移动,同时化学平衡常数K减小
C.达到平衡状态时,增加A物质的量,A和B转化率都提高
D.当各物质浓度满足c(A)=2c(B)=c(C)时,该反应达到了平衡状态
下列离子方程式的书写与所得结论均合理的是
| 选项 |
离子方程式 |
结论 |
| A |
AgCl(s)+I-(aq)═AgI(s)+Cl-(aq) |
溶解度:AgI>AgCl |
| B |
Fe2++H2O2+2H+═Fe3++2H2O |
氧化性:H2O2>Fe3+ |
| C |
CO32-+CO2+H2O═2HCO3- |
稳定性:HCO3->CO32- |
| D |
NH3+H3O NH4++H2O NH4++H2O |
得质子能力:NH3>H2O |
下列说法正确的是
| A.7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.2×6.02×1023 |
| B.VL amol•L-1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023 |
| C.标准状况下,22.4L NO和11.2L O2混合后气体的分子总数为1.0×6.02×1023 |
| D.工业用电解法进行粗铜精炼时,每转移1mol电子,阳极上溶解的铜原子数必为0.5×6.02×1023 |
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是
| A.该硫酸的物质的量浓度为9.2mol/L |
| B.配制250mL4.6mol/L的稀硫酸需取该浓硫酸62.5mL |
| C.该硫酸浓度太大,不能用于干燥氨气 |
| D.硫酸的摩尔质量为98g |
验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是
| A.950 mL 111.2 g | B.500 mL 117.0 g |
| C.1000 mL 117.0 g | D.1000 mL 111.2 g |