(共12分)
(1)Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液。
①该Ba(OH)2溶液的物质的量浓度为___________________;
②溶液中由水电离出c(OH―)=______________;
③该浓度Ba(OH)2溶液与某浓度盐酸溶液按体积比1∶9混合后,所得溶液pH=11(忽略体积的变化),该盐酸溶液的pH=____________。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数KW=_____________。该温度___________25℃(填“>”“=”或“<”)。
(3)常温下,将1 mL pH=1的H2SO4溶液加水稀释至100mL,稀释后的溶液中
c(H+)/ c(OH-)=_______________。
难溶化合物的饱和溶液存在溶解平衡,例如:AgCl(s) Ag++Cl-,Ag2CrO4(s)
Ag++Cl-,Ag2CrO4(s) 2Ag++
2Ag++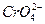 。在一定温度下,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(
。在一定温度下,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(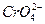 )=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算回答:
)=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算回答:
(1)Cl-、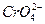 谁先沉淀?
谁先沉淀?
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-的物质的量浓度是多少?(设混合溶液在反应中体积不变)
汽油不完全燃烧的化学方程式为:
2C8H18(l)+23O2(g)====12CO2(g)+4CO(g)+18H2O(l)
人体吸进CO后,CO与人体血红蛋白结合而引起中毒。如果每辆汽车满负荷行驶,每天约有28.5g汽油不完全燃烧。现有200万人口的中等城市,如达到中等发达国家水平,平均每10人拥有1辆汽车。请计算这些汽车满负荷行驶时,每天可产生多少千克CO?
有Fe和Fe2O3混合物溶于500 mL稀HNO3中,放出2.24 L NO(标准状况),并剩余5.44 g Fe。向反应后的溶液中通入2.016 L Cl2(标准状况),恰好能使溶液中Fe2+全部氧化。求:
(1)稀HNO3物质的量浓度。
(2)混合物中的Fe的质量分数。
向由铝粉和过氧化钠组成的混合物中加入足量水,当反应停止后,溶液澄清,共收集到3.5 g气体,向所得澄清溶液中滴加200 mL 3.5 mol·L-1的盐酸,溶液先澄清,然后出现白色沉淀,最后沉淀恰好溶解。求原混合物中铝和过氧化钠各多少克。
某元素X构成的气态单质分子(双原子分子)有三种,其相对分子质量分别为70、72、74,标准状况下,V升该气体中此三种分子的物质的量之比为9∶6∶1。完成下列问题:
(1)X元素有___________种同位素。
(2)各种同位素的质量数分别为___________。
(3)X2的平均相对分子质量为___________。
(4)质量数较小的X原子的物质的量分数为___________。
(5)该气体的质量为___________g。