离子方程式H++OH-===H2O可表示强酸和强碱生成可溶性盐这一类中和反应。下列物质间的反应能用该离子方程式表示的是
①稀H2SO4+Ba(OH)2溶液 ②澄清石灰水+稀HNO3
③稀HNO3+Cu(OH)2 ④醋酸和KOH ⑤Ba(OH)2溶液+稀HNO3 ⑥盐酸+氨水
| A.只有②⑤ | B.除③④⑥ | C.只有⑤ | D.除④ |
化学与生活密切相关,下列说法正确的是
| A.福尔马林可用于保存海鲜产品 |
| B.鸡蛋清中加入CuSO4溶液会发生变性 |
| C.合成橡胶与光导纤维都属于有机高分子材料 |
| D.丝绸和棉花的组成元素相同,分子结构不同,因而性质不同 |
下列各组物质中,互称为同分异构体的是( )。
| A.水与冰 | B.O2与O3 |
C.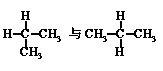 |
D.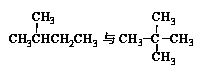 |
下列各组物质中,均能发生水解反应的是( )。
| A.蛋白质和氨基酸 | B.油脂和蛋白质 | C.纤维素和葡萄糖 | D.淀粉和果糖 |
下列对能量转化的认识中,不正确的是( )。
| A.电解水生成氢气和氧气时,电能主要转化为化学能 |
| B.风力发电时,风能主要转化为电能 |
| C.煤燃烧时,化学能主要转化为热能 |
| D.白炽灯工作时,电能全部转化为光能 |
下列化学用语表达正确的是
| A.一氯乙烷的结构式为CH3Cl | B.丁烷的结构简式为CH3(CH2)2CH3 |
C.四氯化碳的电子式为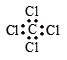 |
D.苯的分子式为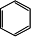 |