已知Na的化合价只有+1价,对于NaH+H2O===NaOH+H2↑下列说法正确的是
| A.H2都是还原产物 | B.H2都是氧化产物 |
| C.NaH中的氢元素被还原 | D.氧化产物与还原产物的质量相等 |
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量水能使溶液恢复到电解前的浓度的是
| A.AgNO3 | B.Na2SO4 | C.CuCl2 | D.HCl |
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,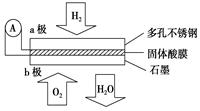
电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-===4OH- |
| C.每转移0.1 mol电子,消耗标准下1.12 L的H2 |
| D.H+由b极通过固体酸电解质传递到a极 |
下列说法正确的是
| A.铅蓄电池放电时铅电极发生还原反应 |
| B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠 |
| C.给铁钉镀铜可采用CuSO4作电镀液 |
| D.生铁浸泡在食盐水中发生析氢腐蚀 |
某蓄电池放电、充电时的反应为Fe+Ni2O3+3H2O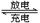 Fe(OH)2+2Ni(OH)2
Fe(OH)2+2Ni(OH)2
下列推断中正确的是
①放电时,Fe为正极,Ni2O3为负极
②充电时,阴极上的电极反应式是:Fe(OH)2+2e-===Fe+2OH-
③充电时,Ni(OH)2为阳极
④该蓄电池的电极必须是浸在某
种碱性电解质溶液中
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
烧杯A中盛放0.1 mol·L-1的H2SO4溶液,烧杯B中盛放0.1 mol·L-1的CuCl2溶液(两种溶液均足量),装置如图所示,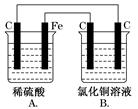
下列说法正确的是
| A.A为电解池,B为原电池 |
| B.Fe电极发生还原反应 |
| C.当A烧杯中产生0.1 mol气体,B烧杯中产生气体也为0.1 mol |
| D.一段时间后,B烧杯中溶液的浓度增大 |