现有MgCl2和Al2(SO4)3的混合溶液,向其中逐滴加入NaOH溶液,得到沉淀的物质的量与加入NaOH的物质的量关系如图所示,
则原溶液中Cl-与SO42-的物质的量之比为
| A.1:3 | B.1:6 | C.3:2 | D.2:3 |
下列关于碳酸钠和碳酸氢钠的比较中,正确的是
| A.相同温度下,在水中,碳酸氢钠的溶解度大于碳酸钠的溶解度 |
| B.将石灰水加入碳酸氢钠溶液中不产生沉淀,加入碳酸钠溶液中产生白色沉淀 |
| C.将100 mL 0.10 mol/L盐酸溶液分别逐滴滴入到10 mL 1.00 mol/L的碳酸钠溶液或10 mL 1.00 mol/L碳酸氢钠溶液中,两者都能放出二氧化碳气体,但碳酸氢钠与酸反应产生二氧化碳的剧烈程度明显强于碳酸钠 |
| D.在一定温度下,物质的量浓度相同时,碳酸氢钠溶液的碱性弱于碳酸钠溶液 |
某氯原子的质量为a g , C-12原子的质量为b g,用NA表示阿伏加德罗常数,下列说法中不正确的是
A.则该氯原子构成氯分子的相对分子质量为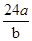 |
| B.1 mol该氯原子的质量为aNA g |
C.m g该氯原子的物质的量为 mol mol |
D.n g该氯原子所含的电子数为 |
下列离子方程式正确的是
| A.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
B.惰性电极电解氯化钠溶液:2Cl- +2 H2O  Cl2 ↑+H2 ↑+2OH— Cl2 ↑+H2 ↑+2OH— |
| C.Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+2OH-=CaCO3↓+CO32- +2H2O |
| D.向Fe(OH)3悬浊液中加入醋酸:Fe(OH)3+3H+=Fe3++3H2O |
根据
(1)Fe+Cu2+=Fe2++Cu (2)2Fe3++Cu=Cu2++2Fe2+
(3)2Fe2++Cl2=2Fe3++2Cl- (4)HClO+H++Cl-=H2O+Cl2,
可以判断出各粒子的氧化性由强到弱的顺序正确的是
| A.HClO>Cl2>Fe3+>Cu2+ | B.Cl2>HClO>Fe3+>Cu2+ |
| C.Cl2>Fe3+>HClO>Cu2+ | D.HClO>Cl2>Cu2+>Fe3+ |
下表为各物质中所含的杂质以及除去这些杂质选用的试剂或操作方法,正确的一组是
| 物质 |
杂质 |
除杂试剂或操作方法 |
|
| ① |
酒精 |
水 |
蒸馏 |
| ② |
H2 |
CO2 |
通过盛有NaOH溶液洗气瓶,再通过盛有浓硫酸洗气瓶 |
| ③ |
NaNO3 |
CaCO3 |
溶解、过滤、蒸发 |
| ④ |
NaCl |
I2 |
加热 |
| ⑤ |
KNO3溶液 |
AgNO3 |
加入NaCl溶液,过滤 |
A. ① ④ ⑤ B. ③ ④ ⑤ C. ① ② ③ ④ D. ① ② ③ ⑤