(16分) 苹果酸是饮料苹果醋的成分之一。合成聚苹果酸的流程如下: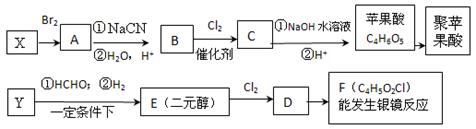
已知:①0.1mol苹果酸与足量碳酸氢钠溶液反应能产生4.48L二氧化碳(标准状况下);
②苹果酸脱水能生成使溴水褪色的产物;
③RC≡CH+HCHO RC≡C-CH2OH;
RC≡C-CH2OH;
④RCH2Br RCH2COOH;
RCH2COOH;
⑤X、Y都是烃,在核磁共振氢谱图上都只有1个峰。
请回答下列问题:
(1)A的名称是__________;C分子中的含氧官能团名称是___________________;
(2)E的结构简式是______________________;
(3)由F制苹果酸可能发生的有机反应类型为___________________;
(4)下列关于苹果酸的说法中不正确的是________;
| A.苹果酸中能发生酯化反应的官能团有2种 |
| B.1mol苹果酸可与3mol NaOH发生中和反应 |
| C.1mol苹果酸与足量金属Na反应生成1mol H2 |
| D.与苹果酸具有相同官能团的同分异构体有2种 |
(5)写出下列反应的化学方程式:
①苹果酸制备聚苹果酸:___________________________________;
②D生成F:_____________________________________________;
(6)B的同分异构体中符合以下条件的有________种。
a.能发生银镜反应;
b.能与碳酸氢钠溶液反应;
c.分子中不存在
(1)现有①苛性钠②碳酸钙固体③酒精④硫化氢⑤三氧化硫⑥金属镁⑦石墨⑧NH3·H2O,其中(填序号)属于强电解质的是,属于弱电解质的是,属于非电解质的是,既不是电解质,又不是非电解质的是。
(2)用pH试纸测定溶液的pH,正确操作是。
用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③酒精灯;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器(填编号)。
(2)应称取Na2CO3的质量为g;若称量时砝码和物品放反了,则实际称量的Na2CO3的质量为g 。
(3)下列操作,会引起所配溶液浓度偏高的是()
| A.称取的Na2CO3固体中有杂质 |
| B.溶解Na2CO3固体时,因搅拌剧烈使烧杯中的溶液溅出少量 |
| C.没有洗涤烧杯及玻璃棒 |
| D.定容时发现液面高于刻度线,用胶头滴管吸出多余的溶剂 |
E、定容时仰视刻度线
F、定容时俯视刻度线
G、定容摇匀后,发现液面低于刻度线,再加至刻度线
(4)取所配Na2CO3溶液20ml,向其中滴加足量的稀盐酸,可得到标况下的气体L,将得到的气体全部通入足量的澄清石灰水,充分反应后,将沉淀过滤,洗涤,干燥,最后可得固体g。
(12分)现有失去标签的CaCl2、AgNO3、HCl、和Na2CO3四瓶溶液。为了确定四种溶液的成分,将它们编号为A、B、C、D后进行化学实验。实验记录如下:
| 实验顺序 |
实验内容 |
实验现象 |
| ① |
A + B |
无明显现象 |
| ② |
B + D |
有无色无味气体放出 |
| ③ |
C + B |
有白色沉淀生成 |
| ④ |
A + D |
有白色沉淀生成 |
根据上述实验完成下列各小题:
(1)A、B、C、D四瓶溶液分别是(用化学式表示所含溶质)
ABCD
(2)写出B与D反应的离子方程式
写出B与C反应的离子方程式
按要求完成下列各题。
(1)向澄清石灰水中通入CO2(写出离子方程式)
(2)用稀硫酸洗铁锈(Fe2O3)(写出离子方程式)
(3)2Al + 6H+ ="=" 2Al3+ + 3H2↑(写出对应的化学方程式并用双线桥法标出电子转移情况)
(8分)中华民族在世界冶金史上曾谱写过辉煌的篇章,早在两千多年前的西汉时期就有“曾青得铁则化为铜”的记载,这种方法是现代湿法冶金的先驱.硫酸铜溶液遇到金属铁时,铁与硫酸铜发生置换反应能生成金属铜,该反应的化学方程式为Fe+CuSO4=Cu+FeSO4.
其中被还原的元素是,被氧化的元素是,氧化剂是,还原剂是,氧化产物是,还原产物是,每得到128克铜时,转移电子数目为。