某同学用电解原理设计一个观察Fe(OH)2沉淀和Fe(OH)2被氧化的实验装置。如图所示,有关该装置的说法正确的是
| A.断开K2 ,接通K1 ,铁棒和石墨棒上都放出大量气泡,两电极附近溶液颜色均无变化 |
| B.断开K2 ,接通K1 ,仅石墨捧上放出大量气泡,石墨电极附近溶液变红,一段时间后水槽中可见白色沉淀生成且保持较长时间不变色 |
| C.断开K2,接通K1,一段时间后再断开K1,接通K2,由于苯层的保护作用,白色沉淀仍能长时间保持不变色 |
| D.若先断开K1,接通K2,铁棒和石墨棒上都放出大量气泡,石墨电极附近溶液变红 |
在密闭容中发生下列反应aA(g)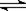 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
| A.A的转化率增大 | B.平衡向正反应方向移动 |
| C.D的体积分数变大 | D.a < c+d |
在容积相同的A、B两个密闭容器中,分别充入2molSO2和1molO2,使它们在相同温度下发生反应:2SO2+O2 2SO3并达到平衡。在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡。在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
A.25% B.大于25% C.小于25% D.12.5%
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g). △H=-1025kJ/mol,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是 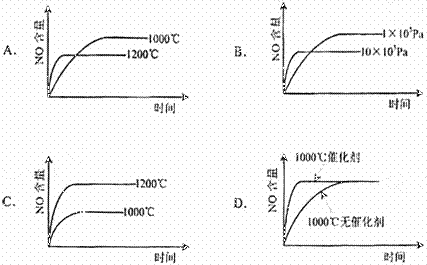
用蒸馏水稀释0.1mol/L的醋酸至0.01mol/L,稀释过程中温度不变,下列各项中始终保持增大趋势的是
| A.c(CH3COOH) | B.c(H+) |
C. |
D. |
某反应其△H="=" -122 kJ/mol,∆S="=" 231 J/(mol·K),则此反应在下列哪种情况下可自发进行
| A.在任何温度下都能自发进行 | B.在任何温度下都不能自发进行 |
| C.仅在高温下自发进行 | D.仅在低温下自发进行 |