25 ℃、101 kPa下:①2Na(s)+1/2O2(g)===Na2O(s) ΔH1=-414 kJ/mol
②2Na(s)+O2(g)===Na2O2(s) ΔH2=-511 kJ/mol
下列说法不正确的是
| A.①和②产物的阴阳离子个数比相等 ,均为1:2 |
| B.①和②生成等物质的量的产物,转移电子数相同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)===2Na2O(s) ΔH=-317 kJ/mol |
乙醇分子结构中,各种化学键如下图所示:乙醇在各种反应中断裂键的说明不正确的是
| A.在Cu催化下和O2反应时断裂①,③键 |
| B.和金属钠反应时断裂键① |
| C.完全燃烧时全部断裂 |
| D.与浓H2SO4共热170℃时断裂键②④ |
一定质量的下列各组物质的混合物,不管两者以何种质量比混合,充分燃烧后所生成的H2O的质量都相等,该混合物可能是
| A.乙醇和乙烯 | B.甲醛和葡萄糖 |
| C.乙烯和乙酸乙酯 | D.丙烷和乙醛 |
分子式为C6H14的链烃中,主链有4个碳原子的同分异构体有
| A.1种 | B.2种 | C.3种 | D.4种 |
有一环状化合物C8H8,它不能使溴的CCl4溶液褪色,它的分子中碳环上一个氢原子被氯取代后的有机生成物只有一种,这种环状化合物可能是
A.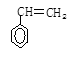 |
B. |
C. |
D. |
某烃分子中有1个环状结构和2个双键,它的化学式可能是
| A.C2H4 | B.C7H8 | C.C5H6 | D.C10H8 |