合成氨的反应为:3H2 + N2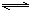 2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1),则下列关系正确的是
2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1),则下列关系正确的是
| A.v(H2)=v(N2)= v(NH3) | B.v(H2)=3 v(N2) |
| C.v(N2)=2 v(NH3) | D.v(NH3)=3/2v(H2) |
下列有关化学用语以及基本概念的表述中正确的一组是
| A.过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团相同,二者互为同分异构体 |
B.碳酸氢钠和亚硫酸氢钠的电离方程式都表示为NaHRO3 Na++HRO3-(R为C或S) Na++HRO3-(R为C或S) |
C.日本福岛核电站泄露的放射性核素 I和 I和 Cs,前者比所有者少4个中子 Cs,前者比所有者少4个中子 |
D.次氯酸的结构式为H-O-Cl,过氧化氢的电子式为 |
2011年12月5日,环保部制定的《环境空气质量标准》第二次公开征求意见结束,大家普遍赞成将PM2.5(PM2.5是指大气中直径接近于2.5×10 -6m的颗粒物)纳入常规空气质量评价。下列有关PM2.5说法不正确的是
| A.PM2.5表面积大能吸附大量的有毒、有害物质 |
| B.PM2.5在空气中形成了气溶胶 |
| C.实施绿化工程,可以有效地防治PM2.5污染 |
| D.研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染 |
.向一定量的 FeO、Fe、Fe3O4、Fe2O3的混合物中加入200ml1mol·L-1的盐酸,恰好使混合物完全溶解,放出224ml(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同的质量的此混合物,能得到铁的质量是
| A.11.2g | B.5.6g | C.2.8g | D.无法计算 |
下列示意图与对应的反应情况正确的是
| A.含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.NaHSO4溶液中逐滴加入Ba(OH)2溶液 |
| C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| D.NaAlO2溶液中逐滴加入盐酸 |

.在某100mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.3mol·L-1和0.1mol·L-1。向该混合液中加入2.56g铜粉,加热,待充分反应后,所得溶液中的Cu2+的物质的量浓度(mol·L-1)是
| A.0.15 | B.0.1875 | C.0.225 | D.0.45 |