Mg—AgCl电池是一种用海水激活的一次电池,在军事上用作电动鱼雷的电源.电池的总反应可表示为:Mg+2AgCl═MgCl2+2Ag下列关于该电池的说法错误的是
| A.该电池工作时,正极反应为:2AgCl+2e-═2C1-+2Ag |
| B.该电池的负极材料可以用金属铝代替 |
| C.有24g Mg被氧化时,可还原得到108gAg |
| D.装备该电池的鱼雷在水中行进时,海水作为电解质溶液 |
下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是()
| A.实验室制乙烯 |
| B.实验室制乙炔并验证乙炔发生氧化反应 |
| C.实验室中分馏石油 |
| D.若A为醋酸,B为贝壳(粉状),C为苯酚钠溶液,验证醋酸、苯酚、碳酸酸性的 强弱(不考虑醋酸的挥发) |
下列说法正确的是()
| A.苯和溴水振荡后,由于发生化学反应而使溴水的水层颜色变浅 |
| B.酸性高锰酸钾溶液和溴水都既能鉴别出甲烷和乙烯,又能除去甲烷中含有的乙烯再经干燥而获得纯净的甲烷 |
| C.煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来 |
| D.石油中含有C5~C11的烷烃,可以通过分馏得到汽油 |
下列说法错误的是()
| A.石油主要是由烃组成的混合物 |
| B.①主要发生物理变化 |
| C.②包括裂化、裂解等过程 |
| D.③是加成反应,产物名称是二溴乙烷 |
在一定条件下,等物质的量的乙烯和苯分别和足量氢气发生加成反应,消耗氢气的物质的量之比为()
| A.1∶1 | B.1∶2 | C.1∶3 | D.1∶4 |
下列反应中,属于取代反应的是()
①CH3CH=CH2+Br2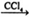 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH 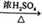 CH2=CH2↑ +H2O
CH2=CH2↑ +H2O
③CH3COOH+CH3CH2OH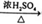 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3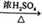 C6H5NO2+H2O
C6H5NO2+H2O
| A.①② | B.③④ | C.①③ | D.②④ |