现取m克铝镁合金与一定浓度的稀硝酸恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到VmL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中正确的有
①沉淀中氢氧根的质量为(n-m)克
②恰好溶解后溶液中的NO3-离子的物质的量为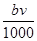 mol
mol
③反应过程中转移的电子数为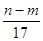 mol
mol
④生成NO气体的体积为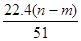 L
L
⑤与合金反应反应的硝酸的物质的量为(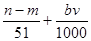 )mol
)mol
| A.2项 | B.3项 | C.4项 | D.5项 |
对溶液中的离子进行鉴定,下列实验所得结论不合理的是
| A.加入稀硝酸后,再加入AgNO3溶液,有白色沉淀生成,则说明原溶液中含有Cl- |
| B.加入KSCN溶液无红色出现,再加入氯水溶液变血红色,说明原溶液中一定含有Fe2+ |
| C.加入用稀硝酸酸化的Ba(NO3)2溶液产生白色沉淀,则可推断原溶液中一定含有SO42- |
| D.加入盐酸产生使澄清石灰水变浑浊的无色无味的气体,可推测原溶液中含有CO32-离子或HCO3- |
有M、R两种主族元素,已知M2-离子与R+离子核外电子数之和为20,下列说法正确的是()
| A.若M在第3周期,则R一定在第2周期 |
| B.M与R的质子数之和为20 |
| C.M2-可能比R+的离子半径小 |
| D.M与R的原子序数之差可能等于7 |
40mLNO、O2混合气体通入到足量的NaOH溶液中充分反应后,溶液中只有NaNO2和NaOH,若剩余气体5mL,则原混合气体中的NO体积为
| A.20mL | B.25mL | C.28mL | D.33mL |
在一定条件下,RO3n—和氟气发生如下反应:RO3n—+F2+2OH—RO4—+2F—+H2O,从而可知在RO3n—中,元素R的化合价是
| A.+4 | B.+5 | C.+6 | D.+7 |
根据以下四个反应:(1)H2S+I2=2H++2I-+S¯(2)H2SO3+2H2S=3S¯+3H2O
(3)2I-+Br2=2Br-+I2(4)H2SO3+I2+H2O=H2SO4+2HI
确定Br-、I-、H2S和H2SO3还原性由强到弱的顺序是
| A.H2S>H2SO3>I->Br- | B.Br->I->H2SO3>H2S |
| C.H2SO3>H2S>Br->I- | D.I->Br->H2S>H2SO3 |