某学生用质量为a g、边长为b cm的正方形均匀镀锌铁片与适置盐酸反应测定镀层厚度,并将实验过程绘图示意,反应至t2时刻时,铁片质量为c g(已知锌的密为 g/cm3)。下列叙述错误的是
g/cm3)。下列叙述错误的是
| A.t1时刻锌镀层已完全反应 |
| B.反应放热也是影响OA段的反应速率的因素之一 |
C.锌镀层的厚度为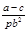 |
| D.过程中有原电池反应发生,负极的电极反应式为Zn - 2e= Zn2+ |
某非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素说法正确的是:
| A.在自然界中只以化合态的形式存在 |
| B.单质常用作半导体材料和光导纤维 |
| C.最高价氧化物不与任何酸反应 |
| D.高温下与C反应生成该非金属单质和CO2 |
下列有关NaHCO3和Na2CO3性质的比较中,正确的是
| A.热稳定性:Na2CO3<NaHCO3 |
| B.常温时在水中的溶解度:Na2CO3<NaHCO3 |
| C.等质量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的量:Na2CO3<NaHCO3 |
| D.等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应,NaHCO3放出的CO2多 |
把过氧化钠投入含有HCO3-、Cl-、Mg2+、Na+的水溶液中,离子数目不变的是
| A.HCO3- | B.Cl- | C.Mg2+ | D.Na+ |
自来水可以用氯气消毒、某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是 ①AgNO3 ②FeCl3 ③AlCl3 ④ NaOH ⑤FeCl2 ⑥Na2CO3
| A.①②⑥ | B.③④ | C.②③ | D.④⑤⑥ |
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于3 区域的是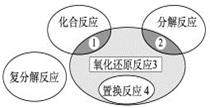
| A.Cl2+2KBr |
B.2NaHCO3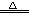 Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
| C.4Fe(OH)2+O2+2H2O |
| D.2Na2O2+2CO2 |