下列事实不能用勒沙特列原理解释的是
A.合成氨反应:N2(g)+3H2(g) 2NH3(g);△H<0,为使氨的产率提高,理论上应采取低温高压的措施 2NH3(g);△H<0,为使氨的产率提高,理论上应采取低温高压的措施 |
B.对2HI(g) H2(g)+I2(g)平衡体系增加压强使颜色变深 H2(g)+I2(g)平衡体系增加压强使颜色变深 |
| C.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
D.已知反应2NO2(g) N2O4(g),红棕色气体NO2加压后颜色先变深后变浅 N2O4(g),红棕色气体NO2加压后颜色先变深后变浅 |
有—CH3,— OH,—COOH,—C6H5四种基团,两两结合而成的有机化合物中,水溶液具有酸性的有
| A.3种 | B.4种 | C.5种 | D.6种 |
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列说法正确的是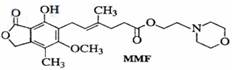
| A.MMF能溶于水 |
| B.MMF能发生取代反应和消去反应 |
| C.1mol MMF能与4 mol氢气发生加成反应 |
| D.1mol MMF能与含6 mol NaOH的水溶液完全反应 |
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是
| 混合物 |
试剂 |
分离方法 |
|
| A |
苯(苯酚) |
溴水 |
过滤 |
| B |
乙烷(乙烯) |
氢气 |
加热 |
| C |
乙酸乙酯(乙酸) |
NaOH溶液 |
蒸馏 |
| D |
淀粉(氯化钠) |
蒸馏水 |
渗析 |
下列分子式表示的物质一定是纯净物的是
| A.C5H10 | B.C7H8O | C.CH4O | D.C2H4Cl2 |
下列各组热化学方程式中,△H1>△H2的是
①C(s)+O2(g)===CO2(g)△H1 C(s)+O2(g)="==CO(g)" △H2
②S(s)+O2(g)===SO2(g)△H1 S(g)+O2(g)===SO2(g)△H2
③H2(g)+O2(g)===H2O(l)△H1 2H2(g)+O2(g)===2H2O(l)△H2
④CaCO3(s)===CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)===Ca(OH)2(s)△H2
| A.① | B.④ | C.②③④ | D.①②③ |