如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是
| A.K1闭合,铁棒上发生的反应为2H++2e-→H2↑ |
| B.K1闭合,石墨棒周围溶液pH逐渐升高 |
| C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D.K2闭合,电路中通过0.4NA个电子时,两极共产生标况下4.48L气体 |
用下列有关实验装置进行相应实验,错误的是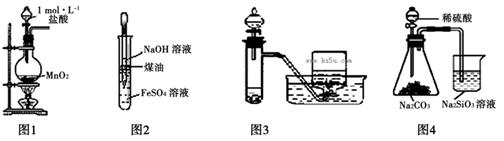
A.用图1所示装置实验室制取少量Cl2
B.用图2所示装置制取及观察Fe(OH)2
C.用图3所示装置用H2O2溶液制备O2
D.用图4所示装置比较S、C、Si的非金属性强弱
下列关于有机物的说法中错误的是
| A.乙烷和乙烯都能与氢气在一定条件下发生加成反应 |
| B.苯和乙烯都能使溴水褪色,但其原理是不同的 |
| C.甲烷和乙醇均能发生取代反应 |
| D.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
下列说法正确的是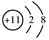
| A.Na的原子结构示意图 |
| B.多电子原子中,在离核较远区域运动的电子能量较低 |
| C.非金属元素组成的化合物中可能有共价键和离子键 |
| D.HF、HCl、HBr、HI的热稳定性和还原性依次增强 |
下列说法中,正确的是
| A.单质Si具有半导体性质,故可用于制作硅整流器、硅太阳能电池 |
| B.将Na2O2投入NH4Cl只可能生成一种气体 |
| C.溶液、胶体和悬浊液的本质区别是分散质微粒是否带电荷 |
| D.氧化铝具有高熔点,用氧化铝制作的坩埚可用来蒸发浓缩烧碱溶液 |
下列有关化学用语的表示,正确的是
A.质子数为92,中子数为146的U原子: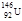 |
B.CCl4分子的比例模型: |
| C.甲醛与醋酸的最简式相同 |
D.2-甲基丁醇的结构简式: |