亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。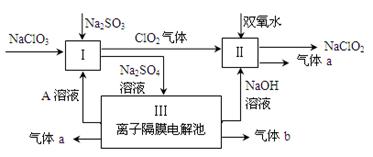
(1)Ⅰ、Ⅲ中发生反应的还原剂分别是 、 (填化学式)。
(2)Ⅱ中反应的离子方程式是 。
(3)A的化学式是 ,装置Ⅲ中A在 极区产生。
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备。写出该制备反应的化学方程式 。
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量 。(填“相同”,“不同”或“无法判断”)
用稀盐酸和氢氧化钡溶液进行酸碱中和反应实验,该反应过程中溶液酸碱度变化及相关数据如右图所示。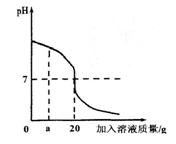
(1)根据此变化曲线,你认为实验操作是将滴加到另一种溶液中。
(2)当加入溶液质量是a g时,溶液中溶质是(写化学式)。
(3)若用pH试纸测定溶液的酸碱度,请写出测定方法:。
(4)当pH=7时,测得生成氯化钡的物质的量为0.05mol,求盐酸中溶质的质量分数?
右图中两圆相交部分(A、B、C、D)可表示铁、稀硫酸、烧碱溶液、硫酸铜溶液间的反应关系,请按下列要求填空:
(1)A处产生的现象是
(2)B处发生反应的类型是;
(3)C处发生反应的化学方程式是 ;
(4)D处发生反应的化学方程式是 。
23.75g某+2价金属氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量_______________MCl2的相对分子质量为_________,M的相对原子质量为_________。
(1)1.5molH2SO4的质量是______g,其中含有_____mol H,含有_______g氧元素。
(2)9.03×1023个氨(NH3)分子含___________mol氨分子,____________mol氢原子,________mol质子,________________个电子。
(3)硫酸铝的化学式为___________,0.2mol硫酸铝中有______molAl3+,__个SO42-。
(4)0.5mol H2O与_________g硫酸所含的分子数相等,它们所含氧原子数之比是_________,其中氢原子数之比是_________。
下列物质中① CO2② HNO3③KOH ④石墨⑤ Fe ⑥葡萄糖⑦Na2CO3⑧酒精⑨食盐水
(1)属于电解质的是_____________________________
(2)属于非电解质的是___________________________
(3)写出电解质的电离方程式